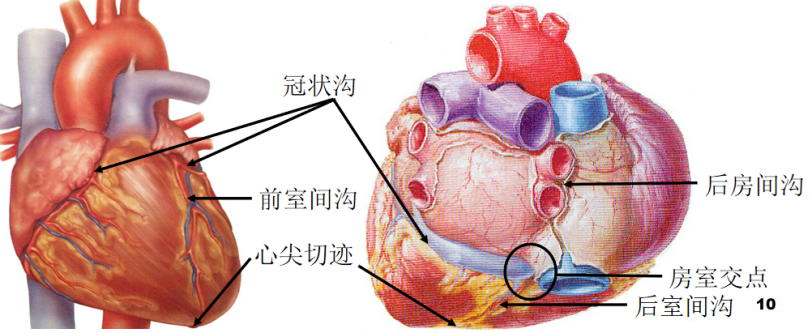
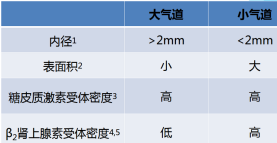
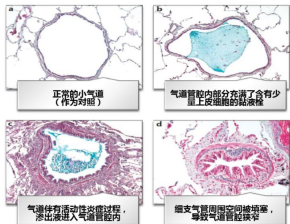
COPD-慢性阻塞性肺疾病
| 概念 |
COPD是一种主要以气流受限为特征,呈进行性发展,不完全可逆,与有害气体或有害颗粒的异常炎症反应有关的一类疾病,其主要病理改变包括慢性支气管炎或(和)肺气肿。
特点:1.气流受限;2.进行性发展;3.部分有可逆性 |
 |
 |
|||
| 病因 | 环境因素 | 吸烟 | 吸烟者患COPD的风险与开始吸烟的年龄、总的吸烟年包数、吸烟的状况等有关,都是COPD死亡率的预测因素。10%~20%的吸烟者最终可能患上COPD |
 |
||
| 空气污染 |
室内空气污染是导致许多发展中国家的一个很重要的危险因素,尤其是发展中国家的女性。
PM2.5 进入呼吸道的颗粒靠粘液–纤毛活动清除;进入肺泡的颗粒由3个途径清除:气道排出、淋巴引流、巨噬细胞吞噬。气体的清除:喷嚏、咳嗽。 |
|||||
| 职业性暴露 | 包括采矿、采石、水泥粉尘、铸造、谷尘、油漆、化工及其他职业粉尘或气体烟雾暴露 | |||||
| 感染 | 流感病毒、鼻病毒、冠状病毒,大都为“自限性”。
“常驻菌”:老年人、慢性病患者及体弱者鼻咽部抵抗力低,甲型溶血型链球菌及奈瑟球菌会突破黏膜屏障,急性支气管炎若不及时适当治疗,就会迁延不愈,变为慢性支气管炎。儿童:反复呼吸道感染 |
|||||
| 个体因素 | 遗传易感基因 | α1抗胰蛋白酶(α1-antitrypsin,α1-AT) 缺乏是迄今为止唯一确定的COPD 遗传易感因素。我国:微粒体环氧化物水解酶、基质金属蛋白酶9启动子基因多态性,与COPD 易感性有关;β-防御素-1基因外显子多态性与南方汉族人群COPD易感性可能有关;
在COPD 发病中可能起重要作用的基因:谷胱甘肽S转移酶M1、基质金属蛋白酶9、组织抑制物2 等基因的多态性变化可能与吸烟人群COPD 易患性的差异有关系。 |
||||
| 气道高反应性 | 与遗传关系较为密切;其机制目前尚不清楚 | |||||
| 其它 | 怀孕期、新生儿期、婴儿期或儿童期由于各种原因导致肺脏发育或生长不良的个体在成人后容易罹患COPD。营养不良、过敏、免疫功能降低和自主神经功能紊乱,平均海拔高度、潮湿寒冷多雾的气候等均与慢性支气管炎的发病有关。 | |||||
| 其它 | 性别、年龄,社会经济地位 | |||||
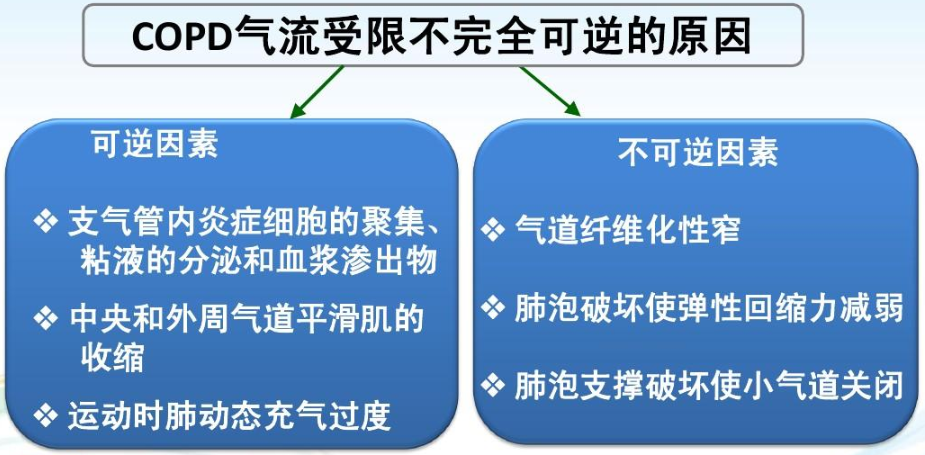
| 发病机制 | 并未完全明确
特征* 1.解剖性气道狭窄 2.肺弹性回缩力下降 |
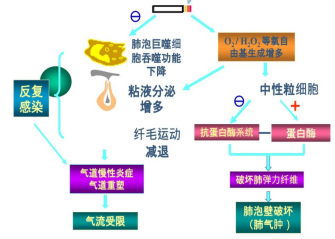
弹性蛋白酶-抗弹性蛋白酶失衡 |
蛋白酶增多,或抗蛋白酶缺乏或相对减少,均可引起蛋白酶/抗蛋白酶失衡,导致肺组织损伤,促使肺气肿的发生。
蛋白酶:包括中性粒细胞弹性蛋白酶(NE)、组织蛋白酶、基质金属蛋白酶(MMPS)等对肺实质有溶解作用 抗蛋白酶:包括al抗胰蛋白酶(al-AT)、分泌型白细胞蛋白酶抑制剂(SLPI)、基质金属蛋白酶抑制剂(TIMPS) 消除蛋白酶的溶解作用 弹性蛋白酶-抗弹性蛋白酶失衡: 患者的炎症细胞可以释放这种弹性蛋白酶,过多的弹性蛋白酶引起肺实质的破坏,产生肺气肿。 在慢性炎症反复侵袭下,肺组织不断损伤,又不断修复。由于炎症等损害因素持续存在,组织修复过程中出现异常生长,如肺泡中的结缔组织纤维发生重塑,发生重塑的组织纤维的硬度和生物力学特性都较正常组织显著下降,肺弹性下降。 |
|||
| 氧化-抗氧化失衡 |
种类:超氧阴离子( O2-) 、羟根(OH) 、次氯酸( HClO) 、H2O2和一氧化氮( NO) 等。
作用:1.破坏生物膜及细胞内成分如蛋白质、脂质和核酸等,导致细胞功能障碍或细胞死亡,破坏细胞外基质,引起蛋白酶-抗蛋白酶失衡。2. 一些祛痰剂减缓COPD的急性发作,减慢肺功能的下降水平正是通过其抗氧化作用实现的。 |
|||||
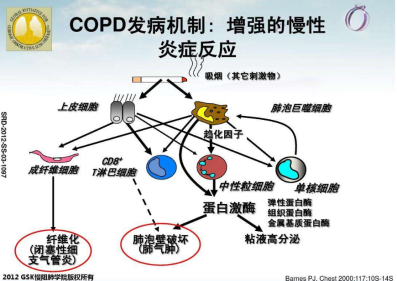
| 炎症-COPD发病的核心 |
肺实质和肺血管的慢性炎症是最重要的机制。
呼吸道具有适当的防御功能,承担起防御功能的结构有: 鼻腔内的鼻毛;咽喉部的正常咳嗽反射; 气管-支气管表面的纤毛和黏液构成的黏液清除系统。 |
 |
||||
| 免疫机制 |
中性粒细胞,巨噬细胞,CD8+。 趋化因子:LTB4:吸引中性粒细胞和T淋巴细胞
IL-8:吸引中性粒细胞和单核细胞 致炎因子:TNF-α,IL-6:放大炎症反应 生长因子:转化生长因子-β:诱导小气道纤维化 |
|||||
 |
||||||
| 主要机能代谢变化 | 血气变化 |
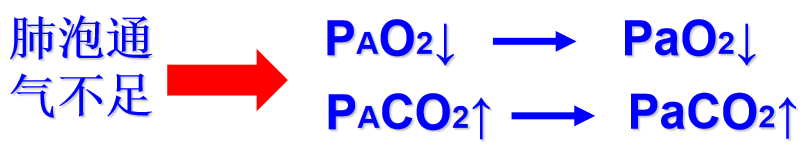 |
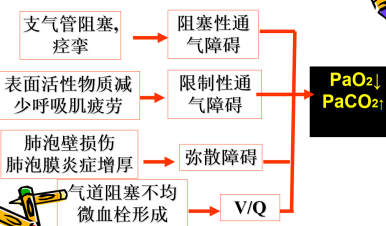 |
|||
| 机能代谢变化 |
早期变化不明显
后期: 呼气性呼吸困难(呼气相阻塞加重;等压点上移)缺氧,酸碱平衡紊乱,肺动脉高压、肺源性心脏病 酸碱平衡及电解质紊乱 代谢性酸中毒:严重缺氧、肾功能不全所致 呼吸性酸中毒:CO2潴留引起 混合性酸碱失衡最多见!呼吸性酸中毒也常见! 肺源性心脏病(右心衰竭) 1.肺动脉高压→右心负荷过度:肺血管收缩;肺小血管重建 2.缺氧酸中毒→心肌舒缩功能障碍 3.用力呼吸时心脏受压→心脏舒张受限度 |
|||||
| 防治原则 |
健康教育与管理:缩短发作期,延迟缓解期
扩张支气管,消炎,祛痰 其它:氧疗、免疫治疗 对症支持治疗 |
|||||
病例讨论
典型病例Ⅰ
女性,78岁,十三年前因受寒引起咳嗽、咳痰,此后,每逢冬季就发作频繁咳嗽,发作呈阵发性,日轻夜重,伴有白色泡沫痰;八年前出现活动气急;本次入院前感胸闷、心悸、气急,四天前突然烦躁不安,神志不清,呼吸急促,紫绀,颜面及下肢水肿,收住入院。
入院检查:T 36.5 ℃,P 90次/分,R 24次/分,BP 110/90mmHg。颈静脉怒张,肝颈返流征(+),桶状胸,两肺叩诊清音,听诊肺底部有湿罗音,心界叩诊缩小,听诊早博 5-6次/分,肝肋下三指,下肢凹陷性水肿,胸片显示两肺纹理增多。
实验室检查:正常血钾(3.5-5.5)K+ 2.8 mmol/L,Na+120 mmol/L,Cl- 80 mmol/L,PaO2 39.6mmHg, PaCO2 71.1mmHg,[HCO3-] 33 mmol/L, BE +2.6 mmol/L,PH 7.26。
思考题:1、患者可诊断为呼吸衰竭吗?依据?
2、该患者发生了何种酸碱紊乱?
3、该患者存在哪些病理生理过程?
A:
1.患者诊断为型呼吸衰竭,依据:血气:PaO2 39.6mmHg, PaCO2 71.1mmHg
2.慢性呼吸性酸中毒急性发作,代偿性:
判断步骤:
1)PH 7.26: 酸中毒
2)PaCO2 原发性 71.1mmHg(肺心病病史13年):呼吸性酸中毒
3)慢性呼酸代偿公式:0.35 X (71.1-40) +- 3 = 10.9 +- 3
实际[HCO3-] 9 mmol/L (33-24),结合病史, 为慢性呼吸性酸中毒
三、病理过程
水肿、低钾血症、呼吸性酸中毒(慢性)、缺氧、呼吸衰竭(慢性,II型)、心力衰竭、应激
病例Ⅱ
48岁,男,因气促、神志模糊送来急诊;活动时呼吸困难已数年,夜间有时感觉憋气,近来活动减少,医生说他有心扩大和高血压,用过利尿剂和强心药。数次急诊为“支气管炎和肺气肿”吸入平喘药,一天吸烟一包已20年,一向稍胖,近6个月长18公斤。
检查: 肥胖、神志恍惚、反应迟钝、不回答问题,无发热,脉搏110,血压 170/110mmHg,呼吸18,打磕睡时偶闻鼾声,肺散在哮鸣音、心音弱,颈静脉怒张,外周水肿。 动脉血PaO2 50 mmHg,PaCO2 65 mmHg, pH 7.33,Hct 49% (40-50) ,WBC计数分类正常, X光肺野清晰,心脏大,肌酐2.6mg/dl(1-2),BUN 65mg/dl(9-20)。
吸氧,用平喘药,作气管插管后送ICU。因发作性呼吸暂停伴血氧降低, 行机械通气。超声心动图见右心肥大与扩大,室间隔运动减弱。肺动脉收缩压70mmHg (18-25)。 在ICU头二天尿增多,BUN及肌酐下降。第三天清醒能正常回答问题。第4天拔去插管,用多导睡眠图测得入睡数分钟出现阻塞性和中枢性呼吸暂停,约每小时30次,最长停38s(15),SaO2常降至58%。持续正压通气可解除阻塞,中枢性呼吸暂停和低氧血症仍存在。再增加吸氧则消除低氧血症。转入普通病房及回家后,每晚仍用持续正压通气和氧疗, 神经症状改善,继续尿多、体重下降。三个月后超声心动图右心已缩小,室间隔运动正常,肺动脉压45/20mmHg (18-25/ 6-10)。
1.试阐述患者发生的呼吸衰竭的类型及主要发生机制。
2.患者是否有肺动脉高压,试阐述其发生机制。
3.试阐述患者发生的酸碱平衡紊乱的类型及诊断依据。
4.分析患者出现了哪些主要的病理过程。
A:
II型呼衰:机制(通气不足,通气/血流比例失调:死腔样通气,功能性分流。判断依据:PaCO2的上升程度与PaO2下降程度不成比例,即呼吸商< 0.8
肺动脉高压:肺血管收缩;肺小动脉重塑;肺毛细血管床减少
肺心病:
右心衰:脉搏加快,紧张源性扩张,心肌肥大,水钠潴留,血流重新分布
肺性脑病:
水肿:心性水肿水钠潴留的发生机制
缺氧 (低张性,循环性)
急性功能性肾功能衰竭 (肾前性):氮质血症,治疗后尿量有增多,右心衰导致心输出量下降所致
酸中毒(呼酸,代酸):
应激:
内科部分
慢性阻塞性肺疾病:持续气流受限,进行性发展,异常慢性炎症反应。临床主要表现为慢性咳嗽、咳痰(或无),胸闷、进行性的活动后气促及肺外表现。每年发病持续3个月或更长时间,连续2年或以上,并排除具有咳嗽、咳痰、喘息症状的其他疾病(如肺结核、肺脓肿、尘肺、支扩、哮喘、慢性鼻咽炎、GERD、心脏病等)
2023版:慢阻肺是一种异质性的肺部疾病,其特征是由于呼吸道异常(支气管炎、毛细支气管炎)和/或肺泡(肺气肿)引起的慢性呼吸道症状(呼吸困难、咳嗽、咳痰),这些异常导致持续的、反复恶化的气流阻塞通常是进行性的气流阻塞。
自主神经系统功能紊乱
1.皮损伤裸露感受器,刺激阈值下降,对烟雾等刺激敏感性增高
迷走神经释放乙酰胆碱增加
2.对突胆碱能神经调节增强
气道慢性炎症至气道上触前受体的功能异常,抑制乙酰胆碱释放的负反馈作用减弱(如肾上腺素能受体)
3.抑制性非肾上腺能非胆碱能神经功能障碍血管活性肠肽(VIP)分泌减少,导致乙酰胆碱释放增加。
4.基础迷走神经张力作用增强,使气道张力作用增加。
5.副交感神经节后纤维释放的乙酰胆碱作用在气道的M受体,M受体的功能、数量异常导致胆碱能神经张力的增高。
病理
病变主要累及中央气道、外周气道、肺实质、肺血管
1.中央气道、外周气道的慢性炎症实质是损伤和修复的反复发生,气道上皮脱落、坏死、粘液分泌的增多,结构重构,疤痕形成,最终导致气道狭窄、气流受阻。
2.肺实质破坏表现小叶中央型肺气肿
病情轻多发生于上肺野,进展后弥漫分布于全肺。
3.肺血管 血管壁的增厚为特征
疾病早期为内膜的增厚,随后出现平滑肌的增生、血管壁的炎症细胞浸润。后期反复COPD加重使血管壁进一步的增厚,导致肺动脉高压。
离不开炎症机制——非特异性炎症
病理生理:高分泌,纤毛功能的失调,气流受限,肺过度充气
气体交换的异常,肺动脉高压和肺心病,全身不良反应
气体陷闭导致肺部过度充气,最终引起呼吸困难症状
无论病情轻重,气体陷闭累及所有COPD患者
三者的区别
1.慢性支气管炎:咳嗽、咳痰,以症状判断为主:气管气道上皮的肿胀、坏死、脱落
2.慢性阻塞性肺疾病:气道的炎症、气流的受限。临床表现:进行性活动后气促,影响肺功能,有其他器官功能的影响。诊断金标准:肺功能(舒张后FEV1/FVC<70%)
3.肺气肿 只是远端的扩张肺泡壁的破坏,但无明显的肺纤维化。一般无明显临床症状
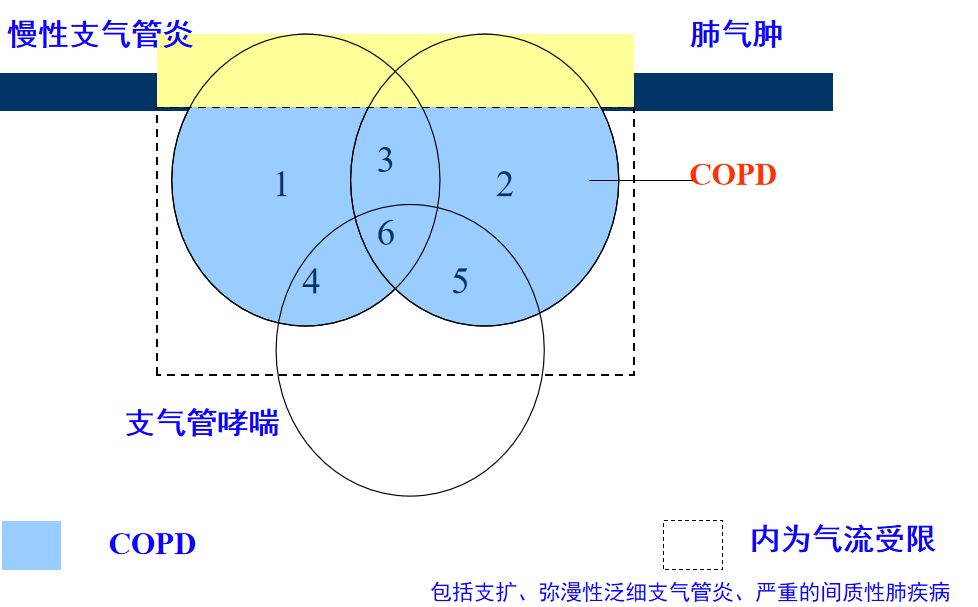
诊断要素
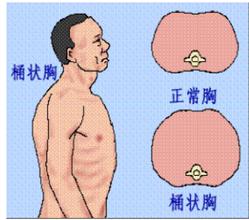
病史 发病的危险因素 烟草、环境、职业污染
临床症状 咳嗽、咳痰(首发),气短或呼吸 困难(标志性)
体征 桶状胸 叩诊过清音,肺的呼吸音减弱
胸片、胸部CT,肺功能,血气分析

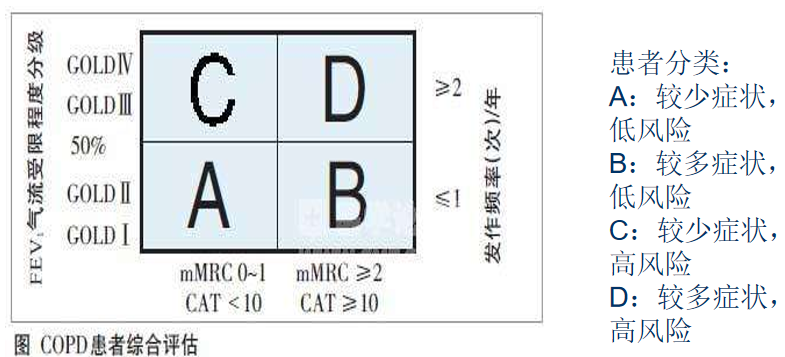
慢阻肺急性加重
COPD鉴别诊断
| 哮喘 | 充血性心衰 | 支气管扩张 | 结核 | 闭塞性细支气管炎 | 弥漫性泛细支气管炎(DPB) |
|
早年发病(常在儿童期)
每日症状变化大 夜间或清晨有症状 过敏症,鼻炎湿疹 家族史 |
胸X线:心影扩大,肺水肿
肺功能容量受限,无气流受限 |
大量脓痰
常伴细菌感染 听诊粗湿罗音,杵状指 胸部X线、CT:支气管扩张,管壁增厚 |
任何年龄
胸部X线:浸润性,结节性病灶 微生物检查可确诊 结核好发区 |
发病年龄较轻、且不吸烟;可能有类风湿关节炎或烟
雾接触史、CT在呼气相显示低密度影 |
亚洲人群,大多数为男性非吸烟者;有慢性鼻窦炎;
胸片和HRCT弥漫性小叶中央结节影和过度充气征 |
并发症:1.慢性呼吸衰竭 2.自发性气胸 3.慢性肺源性心脏病
治疗原则
急性加重发作期:一般性处理:吸氧(控制性氧疗)纠正低氧状态,做好气道护理,床旁备吸痰工具,监测生命体征,病情评估(必要的检验、检查)。
抗感染:选用适当抗生素,及时、足量。
控制气道炎症:激素
舒张气道:支气管舒张剂的应用
促进排痰:化痰药,抗氧化
慢阻肺的基石药物?
机械通气:无创辅助通气与有创性通气的选择
一、支气管舒张剂
1.β2受体激动剂:短效、速效、长效
2.胆碱能受体拮抗剂:短效、长效
3.茶碱类
二、糖皮质激素—-炎症机理
三、抗生素
四、其他药物
1. 祛痰 2. 抗氧化—-抗氧化机制 3. 免疫调节剂
4. 疫苗接种 5. 中医治疗
呼吸道感染细菌

| Gr | 肺炎链球菌 | 白喉棒状杆菌 | 肺炎支原体 | 衣原体 |
| 概述 | 常寄居于正常人的鼻咽腔中,形成带菌状态,在机体抵抗力下降时引起疾病。主要引起大叶性肺炎、脑膜炎、支气管炎等。 | 棒状杆菌属种类较多,其中白喉棒状杆菌致病性强,可引起白喉。 | 是一类无细胞壁,呈高度多形性,可通过滤菌器,能在无生命培养基中繁殖的最小原核细胞型微生物。含有DNA和RNA两种核酸。对青霉素有耐药性。 | 真核细胞内寄生,具有独特发育周期,能通过细菌滤器的原核细胞型微生物,归属于细菌学范畴。
共同特性:1.有细胞壁,G-,呈圆形或椭圆形 2.具有独特的发育周期,二分裂方式繁殖3.有DNA和RNA两种核酸4.含核糖体 5.具有严格的细胞内寄生性6.对多种抗生素敏感 |
|
支原体与细菌L型的异同点;相同点:
缺乏细胞壁,形态多样,能通过滤菌器。 固体培养—菌落呈荷包蛋样或颗粒状。临床表现相似—间质性肺炎、泌尿生殖道感染、不育等 不同点:  |
||||
| 生物学性状 | G+,成对排列,菌矛头状:宽端相对,尖端向外。
有厚荚膜,无芽胞,无鞭毛,有菌毛。 生化反应: 分解葡萄糖、乳糖和菊糖(产酸不产气); 胆汁可溶菌(激活自溶酶)。 |
G+,菌体细长微弯,一端或两端膨大呈棒状
排列不规则,呈栅栏状、L或V字形,无荚膜,无芽胞,无鞭毛, 美兰或奈瑟染色,可有异染颗粒 三个不均一:粗细、排列、染色 |
G-,为原核细胞生物中最小的,呈多形性(球形、丝形)Giemsa染为淡紫色,
高度多形性 菌落呈“油煎蛋”状; 能发酵葡萄糖,不能利用精氨酸与尿素;对美蓝、醋酸铊、青霉素不敏感。 支原体的细胞膜分外、中、内三层,内外两层为蛋白及糖类,中层为脂类,主要为磷脂 主要是二分裂 还有分节,出芽,分枝等方式 |
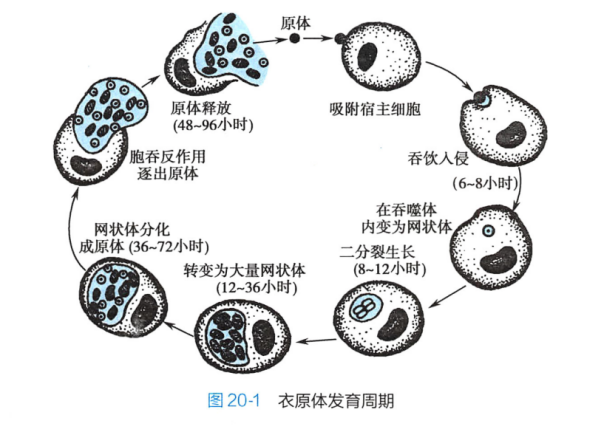
G-,原体(EB)–强感染性,在胞外稳定,无繁殖能力。进宿主易感细胞后,原体在空泡(包涵体)发育成网状体
Giemsa染色紫色,Macchiavello染色红色。 网状体(始体)无胞壁,代谢活跃;二分裂繁殖,在空泡内增殖成许多子代原体;繁殖型,不具感染性,Macchivello染色呈蓝色。 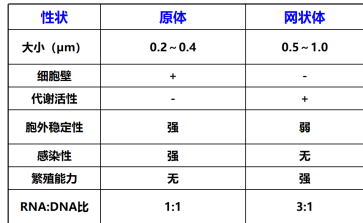 电镜下呈典型的梨形,并有清晰的周浆间隙,Giemsa染色呈紫红色,该法对细胞内包涵体的定位比碘染法敏感 |
| 培养特性 |
营养要求高:血清肉汤;血平板上菌落周围有草绿色溶血圈,a溶血;
产生自溶酶: 固体培养基 —“脐状”菌落 液体培养基 — 浑浊 → 澄清 |
营养要求较高,吕氏血清斜面上生长迅速,异染颗粒明显。
分离培养:鉴别选择培养基(亚碲酸钾)的血平板,黑色菌落。 |
① 营养要求高,需加血清(10-20%)及酵母浸液等。
② PH 7.8-8.0,PH< 7.0死亡 ③ 生长缓慢,菌落小,呈油煎蛋样。 ④ 二分裂繁殖 |
鸡胚接种:6~8日龄鸡胚卵黄囊中繁殖,感染后3~6天致鸡胚死亡,并可在卵黄囊膜中找到包涵体、原体和始体颗粒。
组织细胞培养:可在HeLa、McCoy或HL等细胞中生长良好。 |
| 抗原结构 |
(1) 荚膜多糖抗原:具有型特异性,可将肺炎链球菌分为型。
(2) 其他抗原:C多糖和M蛋白。C反应蛋白(CRP,β 球蛋白)可沉淀C多糖,在炎症活动期(如风湿热)含量增多。 |
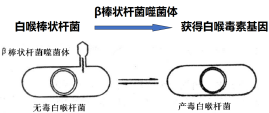
变异性:无毒株携带-棒状杆菌噬菌体时可变异为有毒株
 |
由蛋白质和糖脂组成,交叉较少。
含特殊的顶端结构:P1表面蛋白和P30为主要的粘附蛋白,使肺炎支原体黏附于呼吸道上皮。 |
属特异性抗原:脂多糖,类似于G-菌-补体结合试验检测
种特异性抗原:外膜蛋白(MOMP)上-补体结合试验和中和试验检测鉴别 型特异性抗原:根据MOMP可变区氨基酸序列的不同,分为不同的血清型或生物型(biovar) |
| 抵抗力 | 对理化因素抵抗力较弱,但可抗干燥 | 对湿热抵抗力弱,100℃煮沸1min死亡,对日光和干燥抵抗力强 | 一般与细菌相似,对作用于蛋白质的抗生素敏感 | 衣原体耐冷不耐热。对常用消毒剂敏感,紫外线照射可迅速灭活。四环素、氯霉素、强力霉素和红霉素等抗生素有抑制衣原体繁殖的作用。 |
| 致病物质 | 1. 荚膜:抗吞噬作用,主要毒力因子。
2. 链球菌溶血素O:与细胞膜胆固醇结合,溶细胞;激活补体 ,引起炎症及组织损伤 3. 脂磷壁酸:粘附血管内皮细胞和肺上皮细胞 4. 神经氨酸酶:分解N-乙酰神经氨酸,与细菌的定植、繁殖,和扩散有关 |
白喉毒素:只有携带β棒状杆菌噬菌体的溶原性白喉杆菌才能产生外毒素。
索状因子:破坏易感细胞中的线粒体,影响细胞呼吸与磷酸化 K抗原:抗吞噬作用和利于细菌在黏膜表面定植 不入血 |
顶端结构。肺炎支原体具有超抗原作用,能刺激炎症细胞在感染部位释放大量的淋巴因子(如TNF-α、IL-1、IL-6)引起组织损伤。 | 类似G-菌内毒素的毒性物质,能抑制宿主细胞代谢,直接破坏宿主细胞。
MOMP能阻止吞噬体与溶酶体融合,表位易变异,在体内可逃避特异性抗体的中和作用而继续感染细胞。 热休克蛋白(HSP)能刺激机体巨噬细胞产生TNF-α、IL-1、IL-6等炎症性细胞因子。 |
| 所致疾病 | 大叶性肺炎。还可引起急性或慢性支气管炎、副鼻窦炎、中耳炎和儿童化脓性脑膜炎等。 |
呼吸道传播,儿童易感
咽、喉、气管和鼻腔黏膜 局部渗出的纤维素和白细胞以及坏死组织凝固形成灰白色膜状物(假膜)——窒息,早期死亡原因 心肌炎、软腭麻痹等——晚期死亡原因 A:抑制蛋白合成(酶活性) B:协助A进入细胞,抗体结合 |
原发性非典型性肺炎(间质性肺炎):
临床以咳嗽、发热、头痛、咽痛和肌肉痛为主,有时并发支气管肺炎、皮疹、心血管和神经系统症状。 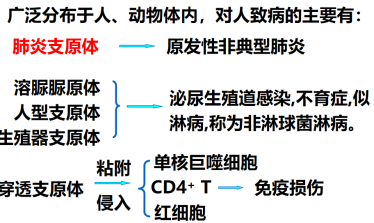  |
易引起肺炎、支气管炎、咽炎和鼻窦炎等。起病缓慢,临床症状与肺炎支原体相似,表现为咽痛、咳嗽、咳痰、发热等,一般症状较轻。
肺炎衣原体与冠心病、动脉粥样硬化等慢性病的发生密切相关,但其具体机制尚待深入研究。 |
| 免疫性 | 建立同型免疫,产生型特异的荚膜多糖抗体 |
抗毒素中和外毒素,感染后可获得牢固的免疫力,
5岁内婴儿易感 |
血清特异性IgM、IgG及SIgA和致敏的淋巴细胞;
呼吸道局部黏膜产生的SIgA对防止再感染有较强保护作用; 出现IgE介导的I型超敏反,促使哮喘病急性发作。 |
|
| 微生物学检查法 |
直接涂片镜检:G+有荚膜的双球菌
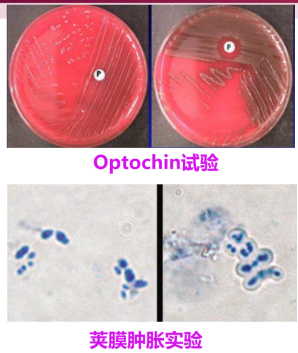
“脐形”菌落;α溶血环 与甲链鉴别: 胆汁溶菌试验 Optochin(奥普托欣)试验 >20mm 荚膜肿胀实验 动物毒力试验 |
锡克试验:24-48h反应阴性时,说明体内有抗毒素,对白喉有免疫力。
方法:注射一定量的白喉毒素于受试者前臂屈侧皮内。 Eleck平板(白喉棒状杆菌毒力试验):接种线两侧距滤纸条约1cm处有无与接种线呈45°角的白色沉淀线出现。 有沉淀线为阳性 |
IgM→支原体
(一)分离培养 痰或咽拭子–SP-4培养基。 初步鉴定:挑选可疑菌落,经形态学、糖发酵、溶血性、血细胞吸附试验进行 进一步鉴定:需用特异性抗血清做GIT与MIT实验。 (二)血清学检查 冷凝集试验 快速诊断:ELISAPCR |
病原学检查:先直接涂片,观察包涵体;以荧光或酶标记的种特异性单克隆抗体直接检测标本中肺炎嗜衣原体抗原。
血清学方法 微量免疫荧光试验(MIF)被称为“金标准”。 |
| 防治原则 |
预防(为主):多价肺炎球菌荚膜多糖菌疫苗
治疗:青霉素G; 万古霉素 |
预防:人工主动免疫:注射白喉类毒素(DPT)
人工被动免疫:注射白喉抗毒素 药物预防:如注射青霉素或口服红霉素 密切接触者:抗生素 治疗:白喉抗毒素,早期足量,抗生素 |
大环内酯类药物:罗红霉素、克拉霉素、阿奇霉素等
喹诺酮类药物:氧氟沙星、斯帕沙星等 |
空气传播
四环素、氯霉素、强力霉素和红霉素等抗生素有抑制衣原体繁殖的作用。 生物型、考拉生物型和马生物型 |
Q

肺炎链球菌的生物学性状;
试述肺炎链球菌的主要致病物质的作用机制
白喉棒状杆菌的形态学特点及其致病机制
肺炎支原体的生物学性状
衣原体与细菌和病毒有何异同点?
原体 (EB)、网状体(RB)
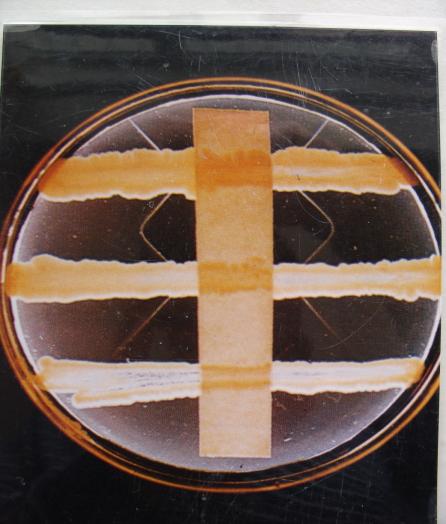
呼吸道感染病毒

| 正粘病毒 | 甲、乙、丙型流感病毒 | 所致呼吸道感染性疾病 |
| 副粘病毒 | 副流感病毒1~5型 | 流行性感冒
普通感冒、支气管炎等 |
| 呼吸道合胞病毒 | 婴儿支气管炎、支气管肺炎 | |
| 麻疹病毒 | 麻疹 | |
| 腮腺炎病毒 | 流行性腮腺炎 | |
| 披膜病毒 | 风疹病毒 | 小儿风疹、胎儿畸形或先天性 风疹综合征 |
| 小RNA病毒 | 鼻病毒 | 普通感冒、急性上呼吸道感染 |
| 冠状病毒 | 普通冠状病毒SARS-CoV SARS-CoV-2 | 普通感冒、急性上呼吸道感染
重症急性呼吸综合征(SARS) 新冠肺炎 |
| 腺病毒 | 腺病毒 | 小儿肺炎 |
|
正粘病毒
| 流感病毒 |
概述 |
对人或某些动物细胞表面的粘蛋白有亲和性,有包膜,具有分节段RNA基因组的一类病毒。只有流行性感冒病毒一个种,包括人流感病毒和动物流感病毒。
有甲、乙、丙三型,甲型是反复流行最为频繁和引起流感全球流行的重要病原体 |
||||
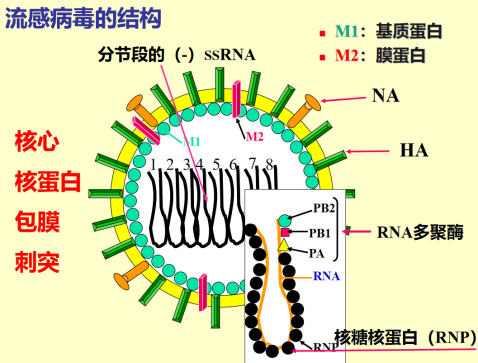
| 形态结构 | 球形,新分离株有时呈丝状或杆状。
有包膜,单链分片段的RNA病毒。 包膜上镶嵌着两种刺突,决定流感病毒的亚型,其抗原性容易发生变异。 血凝素(HA):凝集红细胞,吸附宿主细胞,抗原性(诱导中和抗体) 神经氨酸酶(NA):参与病毒释放,促进病毒扩散,具有抗原性 |
  |
||||
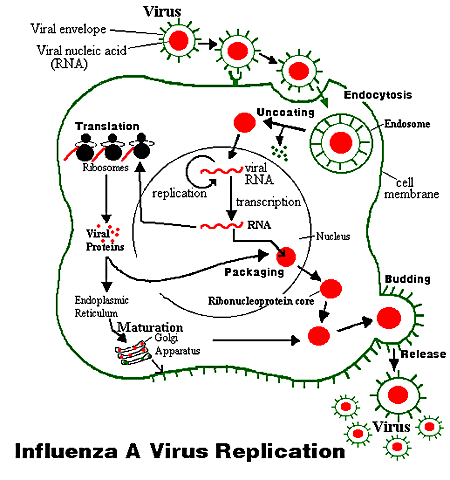
| 复制周期 |
病毒侵入
遗传物质的释放 病毒的复制与病毒蛋白的合成 病毒的装配 出芽 |
 |
||||
| 分型 |
据核蛋白(NP)和基质蛋白(MP)抗原性分:甲型;乙型;丙型
甲型根据HA和NA抗原性不同,再区分为若干亚型:H1~H15;N1~N9 乙型虽有变异,但未划分亚型,丙型未发现抗原变异与新亚型 |
|||||
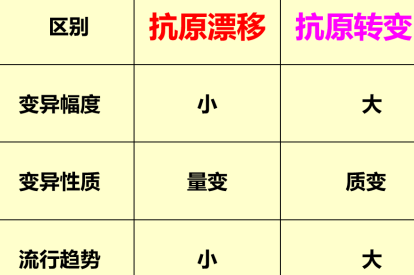
| 抗原变异 | 抗原漂移:因HA或NA的点突变造成,变异幅度小,属量变,引起局部中、小型流行。
抗原转变:因HA或NA的大幅度变异造成,属质变,导致新亚型的出现,引起世界性的暴发流行。 |
 |
||||
| 培养特性 |
最适宜在鸡胚中增殖,但不引起明显的病变。
可进行红细胞凝集实验以确定鸡胚中病毒的存在 |
|||||
| 抵抗力 |
较弱
不耐热,56℃30分钟被灭活。 对干燥、紫外线、乙醚、甲醛等化学药物敏感 |
|||||
| 传染源与途径 |
传染源 —— 病人或病毒携带者
传播途径:病毒经飞沫、气溶胶传播通过呼吸道在人之间直接传播。 |
|||||
| 致病机理 |
病毒HA→呼吸道上皮细胞内增殖→引起细胞变性、坏死、脱落、黏膜充血、水肿等。
神经氨酸酶(NA)可降低细胞表面粘度,使细胞表面受体暴露,便于病毒侵袭 |
|||||
| 临床表现 |
人群普遍易感,潜伏期1-4天
局部症状:鼻塞、咳嗽、流涕、咽痛 全身症状:发热、畏寒、头痛、厌食、乏力、肌肉酸痛 发病初2-3天,分泌物含大量病毒,传染性强。 |
|||||
| 转归 | 自限性疾病,一般于5-7天即可恢复
发病率高、死亡率低 并发症:多见于婴幼儿、老人、慢性病患者 原发性病毒性肺炎,继发细菌性肺炎 急性坏死性脑病心肌炎、心包炎、脓毒性休克 |
|||||
| 免疫性 | 同型有1-2年免疫力
sIgA抗体有短暂阻断病毒感染的保护作用 抗HA特异性抗体为中和抗体,持续时间长 抗NA特异性抗体抑制病毒的释放和扩散 抗NP特异性抗体具有型特异性 体液免疫: CD4+T,B 细胞免疫: CD8+T |
|||||
| 微生物学检查 | 病毒分离
标本:采集发病3 天以内病人的咽洗液或咽拭子 培养:经抗生素处理接种猴肾细胞或鸡胚尿囊腔 结果:红细胞凝集、血凝抑制试验分型 血清学诊断:HI 试验检测抗体效价(双份血清),补体结合试验(CF)检测NP、MP抗体 快速诊断:采用免疫荧光法、 ELISA检测抗原,RT-PCR、核酸杂交等 |
|||||
| 防治 |
灭活疫苗,减毒活疫苗
对症治疗及防止细菌性并发症 药物治疗:盐酸金刚烷胺、奥司他韦、利巴韦林、干扰素滴鼻、板兰根、大青叶 |
|||||
|
副粘病毒
|麻疹病毒 |
概述 |
 |
||||
| 麻疹的病原体。儿童时期最常见的急性传染病。冬春季发病率最高。临床表现以皮丘疹、发热及呼吸道症状为主要特征。麻疹本身可自愈,但常引起严重的并发症而导致死亡,是发展中国家儿童死亡的一个主要原因。 | ||||||
| 形态结构 |
颗粒较大,呈球形或丝形
包膜刺突为血凝素(HA)和溶血素(HL) 核心为完整的不分节段的单股负链RNA,只有一个血清型 |
|||||
| 培养特性 | 可在多种原代或传代细胞中增殖;能使细胞融合成多核巨细胞,核内及胞浆中可出现嗜酸性包涵体;抵抗力弱。 | |||||
| 致病性 |
人是麻疹病毒的唯一自然宿主
急性期患者为传染源:出疹前6天和出疹后3天都有传染性 通过飞沫或鼻腔分泌物传播,也可通过玩具传播 |
|||||
| 致病机理 |
入侵→呼吸道上皮细胞内增殖→入血(第一次病毒血症)→侵入淋巴组织和单核吞噬细胞系统→增殖后再次入血(第二次病毒血症)
→多种组织、器官受累,出现明显的临床症状 |
|||||
| 临床表现 |
潜伏期约10~12天
体温略高、咳嗽、流涕、好打喷嚏及泪眼,症状持续3~5天 体温突然升高(达到40~40.5C),口颊粘膜出现柯氏斑,随后出现红色班丘疹,从耳部开始,2~3天后遍及全身,4天后消退,脱屑 |
|||||
| 并发症 |
呼吸道最为常见,如继发性细菌性肺炎、支气管炎
消化道:腹泻、阑尾炎或盲肠炎 营养失调,脑脊髓炎(0.1%),中耳炎等, 亚急性硬化性全脑炎 (SSPE):少见但严重。慢性进行性(慢发),主要是少年或青年。原因可能是麻疹病毒持续感染:SSPE患者既往都有麻疹感染病史,血清及脑脊液中麻疹病毒抗体滴度高,尸检可在脑部检出大量核内包涵体。为急性病毒感染的迟发并发症,表现为渐进性大脑衰退,一般在1 ~ 2 年内昏迷死亡。 |
|||||
| 免疫力 |
免疫力牢固,抗HA抗体和抗HL抗体可抵御再感染,终生免疫
恢复期主要为细胞免疫 细胞免疫缺陷的麻疹病人预后很差,母亲抗体可保护新生儿 |
|||||
| 微生物学检查 |
病毒分离:复杂费时,临床不用
血清学检查:双份血清 快速诊断:免疫荧光检测病毒抗原 |
|||||
| 防治 |
治疗方法(对症):扑热息痛(即:对乙酰氨基酚)及水疗法控制高热
保持室内湿度,及时补液,注意饮食营养,儿童应补充维生素A,注意并发症 预防:隔离患者,麻疹减毒活疫苗,麻疹-腮腺炎-风疹三联疫苗。 接触后5天内,紧急被动免疫用丙种球蛋白或胎盘球蛋白。 |
|||||
| 冠状病毒和SARS冠状病毒 | 概述 | 单正链RNA,不分节段,螺旋对称,有包膜,突起,对理化因素耐受力差
三个血清型,与鼠肝炎病毒有共同抗原,普遍存在,引起普通感冒和咽喉炎 自限性,飞沫传播 一、冠状病毒:单正链RNA,不分节段,螺旋对称,有包膜,突起 对理化因素耐受力差,三个血清型,与鼠肝炎病毒有共同抗原 普遍存在,引起普通感冒和咽喉炎,自限性,飞沫传播 二、SARS冠状病毒:引起严重急性呼吸综合症(SARS) |
||||
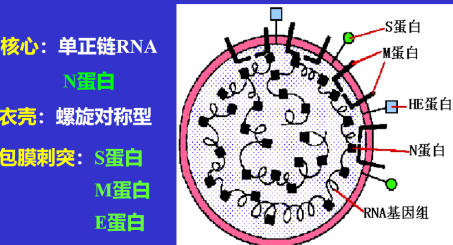
| 形态结构 | 病毒颗粒不规则,有包膜,四周伸出突起,形如花冠。螺旋单正链RNA及衣壳N蛋白组成核衣壳。包膜有E蛋白,且表面有两种蛋白:S蛋白、M蛋白。 受体是血管紧张素酶 2(ACE2) |
 |
||||
| 培养及抵抗力 |
可在Vero-E6细胞,FRhK-4细胞内进行增殖并引起细胞病变。
病毒复制可被恢复期血清所抑制。 对脂溶剂敏感,对热、冷抵抗力较冠状病毒强。 粪便和尿中存活1-2天 |
|||||
| 传染源与传播途径 |
传染源:SARS患者
传播途径:近距离飞沫传播为主,同时可以通过接触病人呼吸道分泌物经口、鼻、眼传播,不排除经粪-口等其他途径传播。 人群普遍易感,在冬、春季流行为主。 |
|||||
| 致病性 |
潜伏期2-10天。
以发热为首发症状,伴头痛乏力、关节痛。 继而出现干咳等肺部病变表现,X胸片48h病灶50%以上,并呈多叶病变。 严重者出现呼吸困难,低氧血症,严重肺渗出,呼吸窘迫,伴过敏性血管炎,休克,DIC,心率紊乱等。 |
|||||
| 免疫性 | 10天出现IgM。15天出现 IgG,具有中和保护作用。同时出现细胞免疫。 | |||||
| 微生物检查 |
病毒分离鉴定:P3 实验室。。采集咽拭子、痰液、气管分泌物等标本,用Vero-E6细胞分离培养病毒。
核酸检测:RT-PCR。。血清学检查:患病12天后检出率高。 |
|||||
| 防治原则 |
预防措施:隔离病人,切断传播途径,提高机体免疫力,SARS特异性疫苗的研制
治疗方法:对症处理支持疗法 |
|||||
| 风疹病毒 | 生物学性状 | 不规则球形,核心为单正链RNA,有包膜。包膜刺突有血凝素刺突,只有一个血清型,人是其唯一自然宿主 | ||||
| 致病性 | 儿童是主要易感者,呼吸道传播,局部淋巴节增殖后经病毒血症散播全身,表现为发热、麻疹样皮疹,并伴有耳后和枕下淋巴结肿大,成人感染症状较重。病后大多预后良好 | 可垂直传播导致胎儿先天性感染,引起流产或死胎,或先天性风疹综合症(CRS),引起胎儿畸形,表现为心脏病、白内障、耳聋三大主症。 | ||||
| 预防及免疫 |
自然感染后可获持久免疫力,母亲抗体可保护胎儿,接种风疹减毒活疫苗
三联疫苗(MMR:麻疹、腮腺炎、风疹)孕妇要进行风疹病毒的检查 |
|||||
|
副流感病毒
包括 | |
生物学性状 |
球形,不分节段-ssRNA核蛋白呈螺旋对称
包膜糖蛋白突起:HN蛋白,F糖蛋白 属副粘病毒科呼吸病毒属和德国麻疹病毒属:5个血清型 尚无有效的疫苗和治疗方法 |
||||
| 致病性与免疫性 |
飞沫传播或直接接触传播
* 仅在呼吸道上皮细胞增殖,不入血 * 上呼吸道感染、婴幼儿严重哮喘、支气管肺炎和肺炎 |
|||||
| 微生物学检查法 |
病毒分离
快速诊断:免疫荧光检测病毒抗原 |
|||||
| 呼吸道合胞病毒 | 生物学性状 |
属副粘病毒科 肺病毒属: 球形
不能在鸡胚培养,但可在组织培养增殖 –胞浆嗜酸性包涵体。一个血清型 |
||||
| 致病性与免疫性 |
流行于冬季、早春,传染性强
* 是医院感染的主要病原之一 * 潜伏期4-5天,排毒可持续1-3周 |
|||||
| 腮腺炎病毒 | 生物学性状 |
属副粘病毒科副粘病毒属:鸡胚羊膜腔增殖
* 一个血清型 人是唯一自然储存宿主 |
||||
| 致病性与免疫性 |
飞沫传播
* 引起流行性腮腺炎 * 病后免疫力持久 可用减毒活疫苗 |
|||||
飓(巨细胞病毒)风(风疹)攻(弓形虫)击单(单纯疱疹病毒)薄的胚胎-导致先天性婴儿畸形
Q
流感病毒的形态结构特点
常见呼吸道感染的病毒及引起疾病?
HA、NA的功能,变异以及与流行的关系。
冠状病毒和SARS冠状病毒的特点
麻疹病毒的致病性和并发症
SARS病毒的致病机制
感染呼吸系统的人体寄生虫
成虫直接寄生呼吸系统:卫氏并殖吸虫(形态、生活史、致病、诊断、流行及防治)
幼虫或原虫滋养体直接寄生在肺部:溶组织内阿米巴、细粒棘球绦虫、蠊缨滴虫 (致病、诊断、流行及防治)
幼虫移行途径肺部:粪类圆线虫、钩虫和蛔虫(致病、诊断)
异位寄生:日本血吸虫(致病、诊断)
幼虫移行症:广州管圆线虫、斯氏狸殖吸虫、棘颚口线虫等
直接寄生呼吸系统的寄生虫
| 卫氏并殖吸虫
卫氏并殖吸虫 |
形态 | 成虫 |
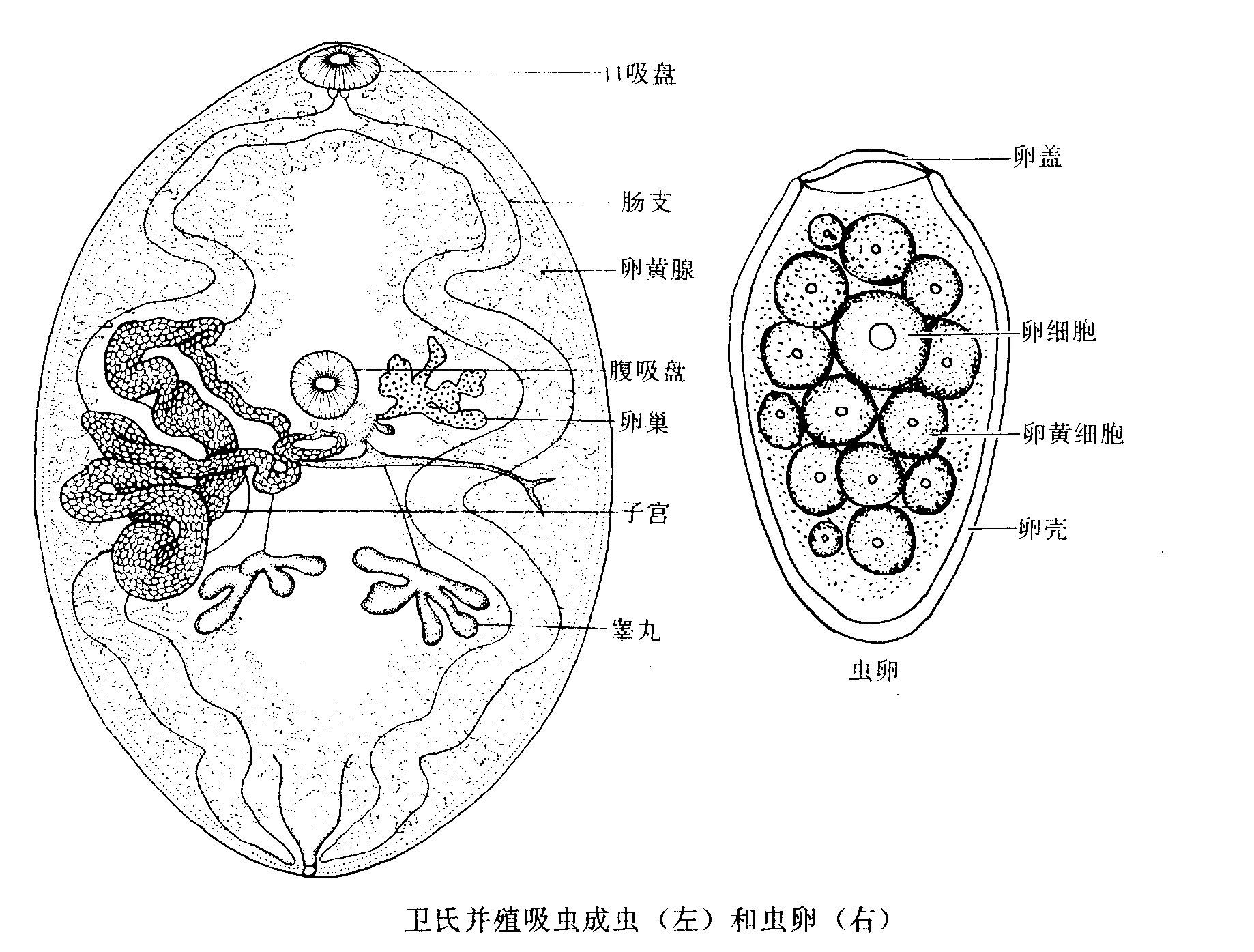
大体:椭圆形,腹扁平背隆起,似半颗黄豆,约10×5×3mm。
镜下:♀♂同体:卵巢与子宫左右并列,两个睾丸左右并列(主要形态特征)。 腹吸盘位于中线前缘。 两个肠支有多个弯曲,延伸至虫体后部,盲端。 |
 |
||||||
| 虫卵 | 金黄色、椭圆形,约100×55um,卵盖大而倾斜(可缺盖),卵壳厚薄不均匀,卵内含一个卵细胞,10多个卵黄细胞。 |
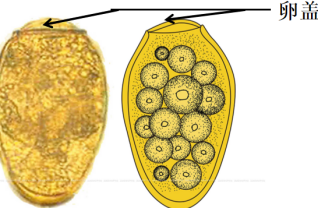 |
||||||||
| 生活史 |
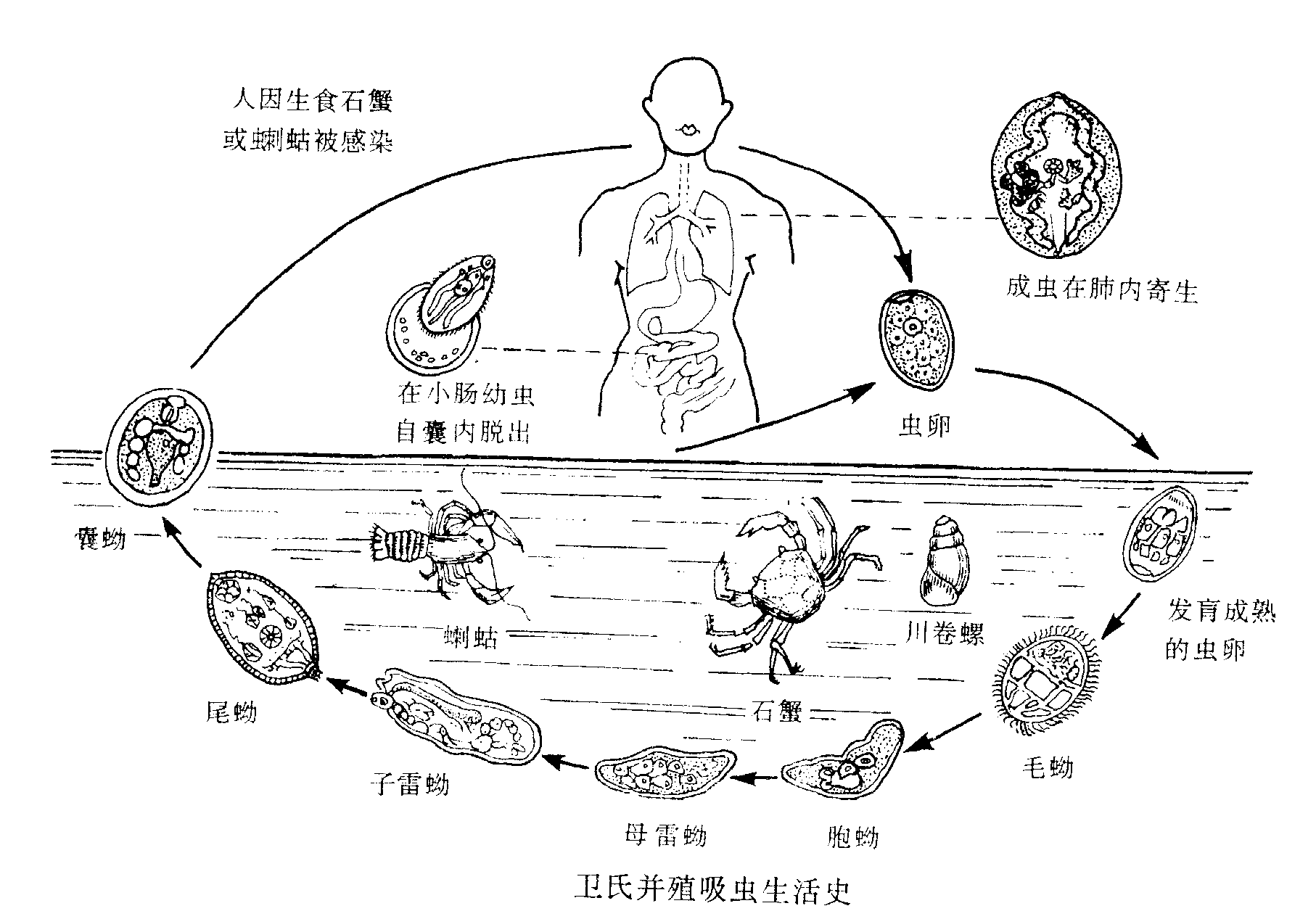 |
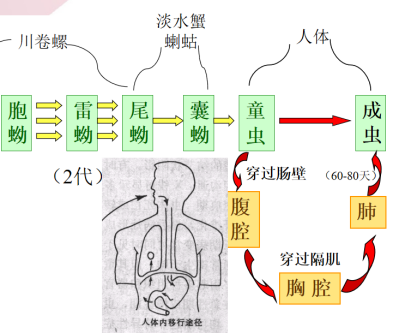 |
||||||||
|
1、寄生部位:肺
2、宿主: 1)终宿主:人 2)保虫宿主:常见虎、豹、猫、狗等 3)转续宿主:野猪、鼠、兔、鸡、鸭、鹅、鹌鹑等 4)第1中间宿主:川卷螺 5)第2中间宿主:溪蟹、 蝲蛄 3、感染阶段:囊蚴 4、感染方式: 1)吃入生的或未熟的含活囊蚴的溪蟹或蝲蛄 2)吃入生的或未熟的含幼虫的转续宿主肉。 3)喝进含囊蚴的生水。(较少见) 5、异位寄生:常见在肝、脑、皮下、腹腔、阴囊及肌肉等 |
||||||||||
|
致病
|主要是成虫 |
病变过程分2期 | 急性期:主要损害肠和肝。由童虫移行、窜扰引起。 |
1.童虫 移行:腹壁 血性或化脓性肌炎,腹腔 血性积液,肠壁粘膜 出血性或脓性窦道
2.童虫 窜扰 :肝局部出血、坏死。 |
|||||||
| 慢性期 :
主要损害肺 肺内典型病变为:(1)囊内出现液面; (2)空囊;(3)多房性囊肿。 |
脓肿期 | 组织破坏、出血、渗出、炎症(X线边界不清,浸润性阴影)–窟穴形成期 | ||||||||
| 囊肿期 | 大量细胞坏死、崩解、液化X线边界清楚的结节状或条索状阴影)赤褐色果酱样液体:坏死组织、虫卵、夏科雷登氏结晶 | |||||||||
| 纤维疤痕期 | 囊内容物排出或吸收,纤维化 | |||||||||
| 临床表现 | 急性期 |
食入囊蚴后数天至1个月出现,可持续1~3个月
非特异性症状:轻重不一,轻者表现食欲不振、腹痛、腹泻、低热等。重者表现高热、胸痛、气促、全身超敏反应。 |
||||||||
| 慢性期 |
(1)胸肺型:以血痰为主要特征,伴咳嗽、胸痛。铁锈色痰。类似结核病。
(2)腹肝型:占1/3,腹痛、腹泻、大便带血等。 (3)皮下型:占10%,以皮下结节或包块为特征,多呈游走现象,好发腹壁、胸背、头颈。 (4) 脑脊髓型:占10-20%,以侵犯部位而定。常见有阵发性,剧烈头痛、 癫痫发作,运动神经障碍如偏瘫、视力障碍等。 (5)亚临床型 :症状不明显,血清免疫学检测阳性。感染早期或者是虫体消失的感染者 (6) 其他型 |
|||||||||
| 诊断 |
病原检查
1、痰液检查(主要方法) 1)痰液直接涂片法查虫卵,2)收集24小时痰液、消化、离心、取沉渣涂片查虫卵 2、粪便检查 1)直接涂片法 2)沉淀集卵法 3、皮下结节或包块活体组织检查:手术找虫体 辅助诊断:1.免疫检查:酶联免疫吸附试验 阳性率90%以上。假阳性。 2. X线、CT检查 |
|||||||||
| 流行 | 分布 | 主要分布在亚洲。广东、山东、四川等,广东主要流行于粤北山区。 | ||||||||
| 因素 |
1. 传染源的存在:病人、带虫者及保虫宿主、转续宿主。
2. 中间宿主的存在:1)第1中间宿主 川卷螺, 2)第2中间宿主 溪蟹、蝲蛄 |
|||||||||
| 不良饮食习惯 |
(1)生吃或半生吃溪蟹或蝲蛄
(2) 通过被囊蚴污染的食具而感染 (3) 生喝含活囊蚴的水 (4) 生吃含幼虫的转续宿主的肉 |
|||||||||
| 防治 |
1. 改变不良饮食习惯(关键)
2. 加强粪管,不随地吐痰,防止虫卵污染水源。 3. 治疗病人、带虫者。处理保虫宿主。 药物有吡喹酮,25mg/kg,tid ×3d |
|||||||||
| 斯氏狸殖吸虫 | 概述 |
一般在人体内不能发育为成虫,主要是童虫寄生或不断移行引起幼虫移行症
成虫虫体窄长,虫体最宽处约在虫体前1/3或稍后;腹吸盘位于体前约1/3处,略大于口吸盘;睾丸左右并列,长形且有分支。  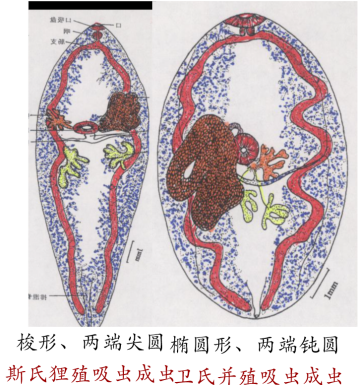 |
||||||||
| 致病 | 1. 皮肤型:游走性结节或包块,多见于腹部、胸部、腰背部等,多为1~3cm。
2. 内脏型:侵犯肺:咳嗽、痰中偶有血丝,胸腔积液,痰中通常无虫卵。 侵犯肝:肝痛、肝肿大等。 血常规:嗜酸性粒细胞明显增高 本病损害器官不定,可同时多个器官受损,易被误诊。 |
|||||||||
| 诊断 |
1.活组织检查—皮下包块
2.免疫学检查 |
|||||||||
| 防治 |
同卫氏并殖吸虫
治疗:首选药物吡喹酮,疗效稍逊于卫氏并殖吸虫吸虫病 |
|||||||||
| 叶足虫
|| 溶组织内阿米巴 |
概念 |
又名痢疾阿米巴,主要寄生于结肠,引起阿米巴痢疾和肠外阿米巴病。
感染后大多处于带囊状态。 |
||||||||
|
形态
| 滋养体 |
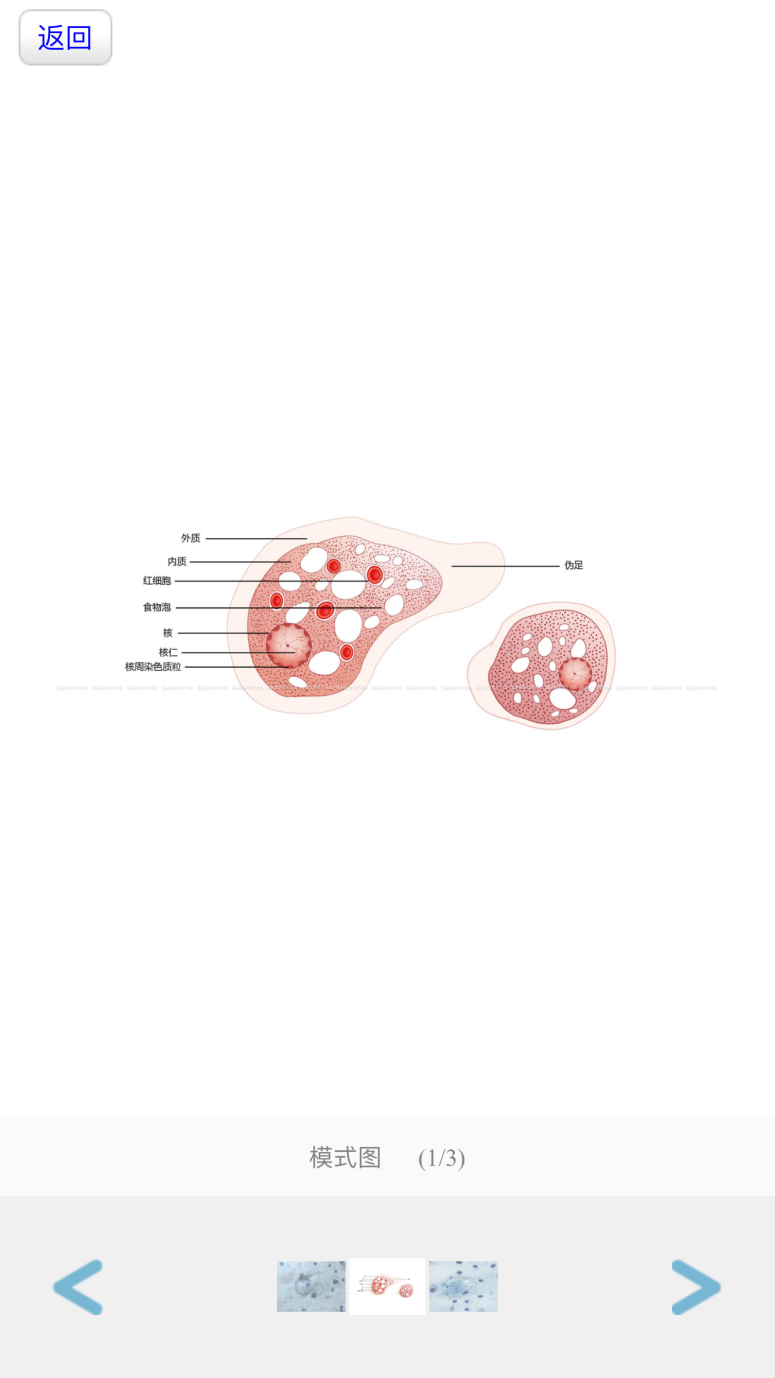
体形不固定,有叶状伪足的运动器官,比白细胞略大,内外质分明,外质透明,内质颗粒状,可见吞噬的红细胞
泡状核,核仁小,居中。核膜内缘有染色质粒,大小一致,均匀排列;核仁与核膜间有时可见网状核纤丝 肥肥的身、小小的核,形态不定随机变 我混杂在细胞中,吞噬异物被误认为巨噬。 |
 |
||||||||
| 生活史 |
1、好发部位:常见盲肠、阑尾,及乙状结肠、升结肠等
2、感 染 期:成熟包囊(四核包囊) 3、感染方式:(主要经口感染) (1)吃入被成熟包囊污染的食物。 (2)喝进被成熟包囊污染的水。 (3)性接触感染 溶组织内阿米巴生活史的基本过程是包囊→肠腔内滋养体→包囊 4、致病阶段:滋养体 (组织内) ①形成包囊,排出体外;②侵入肠黏膜→血行播散→ 肠外寄生 |
|||||||||
| 致病 | 慢性:阿米巴肿–组织肉芽肿伴慢性炎症和纤维化
肠外:经血扩散、侵入肝窦→阿米巴肝脓肿(右叶)→阿米巴肺脓肿 其他:脑、纵膈、心包、脾脓肿、皮肤、阴道、前列腺炎 肠阿米巴病:烧瓶样溃疡 肠外阿米巴病:肝脓肿 |
|||||||||
| 临床表现 |
肠外阿米巴病:阿米巴肺脓肿(多发性肺阿米巴病)
来源:1、肝脓肿穿破膈肌,2、血行播散 表现:1、发热,2、胸痛,3、咳嗽,4、咳“巧克力酱样”痰 |
|||||||||
| 诊断 |
病原诊断
1、生理盐水直接涂片法:用于急性病人,查滋养体 送检材料时要注意3点:(1)粪便要新鲜,取脓血粘液便。(2)注意保温,快速送检。(3)盛器要清洁干净,无尿无药物无消毒液,以免杀灭滋养体。 2、碘液染色法 用于慢性病人,查包囊。3、包囊浓集法 4、体外培养:Robinson培养基,亚急性或慢性 5、核酸诊断 (二)血清学诊断:酶联免疫吸附试验(辅助检查) (三)影像诊断:结肠镜、超声波、CT、X线、磁共振扫描等 |
|||||||||
| 防治 | 治疗病人、带虫者:甲硝唑,替硝唑,巴龙霉素,二氯尼特 | |||||||||
| 细粒棘球绦虫 | 概述 |
又称包生绦虫;
幼虫棘球蚴寄生于人、多种食草类家畜; 引起一种危害严重的棘球蚴病(囊型包虫病)。 |
||||||||
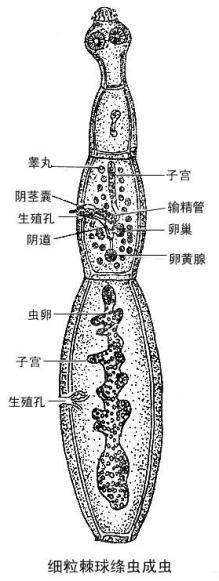
| 形态 | 成虫 | 细粒棘球绦虫:长2-7mm,通常只有四个节片,头节略呈梨形,前端有顶突,伸缩能力强,上有小钩,四个吸盘。 |
 |
|||||||
| 棘球蚴 |
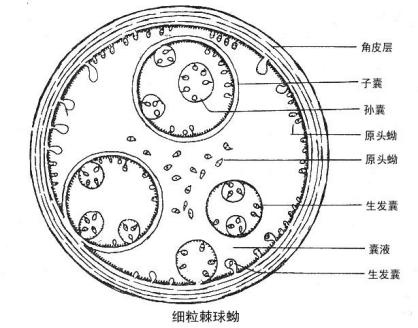
1.大体:圆形囊状体,大小不等,囊内充满液体。囊壁分外层-角皮层,乳白色,半透明。内层为生发层,可向囊内长出许多原头蚴。生发囊其内可长出原头蚴、子囊。
囊壁外有纤维组织包绕。 2. 镜下——棘球蚴砂:脱落于囊内的育囊、子囊、原头蚴统称棘球蚴砂。 |
 |
||||||||
| 生活史 |
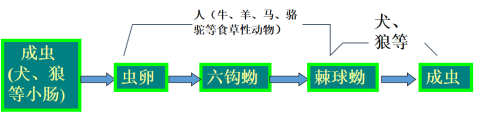 1.棘球蚴在人体的寄生部位(肝>肺>腹腔) 2.终宿主:犬、狼等食肉性动物。 3.中间宿主:人和羊、牛、骆驼等食草性动物。–终→狗小肠 4.感染阶段:虫卵 5.感染方式:经口食入被虫卵污染的食物 |
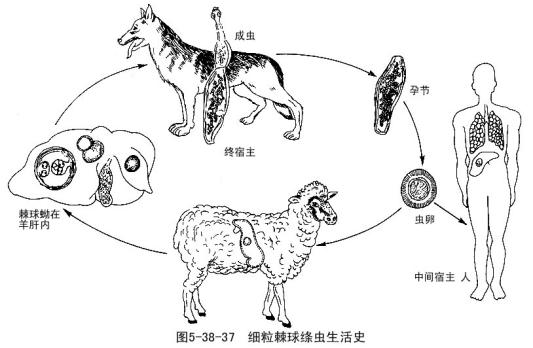 |
||||||||
| 致病 |
可寄生于肺——咳嗽、咯血、胸痛等
若棘球蚴破裂,可咳出生发囊、子囊、角皮碎片 |
|||||||||
| 诊断 |
1.询问病史:是否来自疫区,与动物和皮毛接触史、猎狐等。
2. 病原学诊断:确诊依据是从痰液、尿液、腹水、胸水直接镜检出棘球蚴或棘球蚴砂。阳性率低。禁止穿刺–体内继发感染和过敏性休克 3.免疫诊断 (泡球蚴免疫诊断效果尤佳)(1)检测抗体:ELISA(2)检测抗原 多采用综合方案:2-3项血清学试验以提高诊断准确率。 4. X线、CT |
|||||||||
| 流行与防治 |
1. 分布:世界各地的畜牧区(棘球蚴),北半球高纬度地区(泡球蚴)
2. 流行因素:细粒棘球绦虫:(1)犬科食肉性动物——偶蹄类食草性动物之间相互传播。(2)病畜内脏乱丢。(3)不良卫生习惯。(4)与牧犬、畜接触密切。 3. 防治:(1)严格处理病畜内脏,不乱丢。(2)注意饮食卫生,牧区非常强调洗手。不喝生奶、生水,不吃生菜,饭前洗手等(3)治疗以外科手术为主。 治疗药物:阿苯达唑、吡喹酮等 |
|||||||||
| 蠊缨滴虫 | 概述 | 主要寄生于白蚁和蜚蠊的消化道,可侵袭人体呼吸系统,是一种新现的寄生虫病。 | ||||||||
|
形态
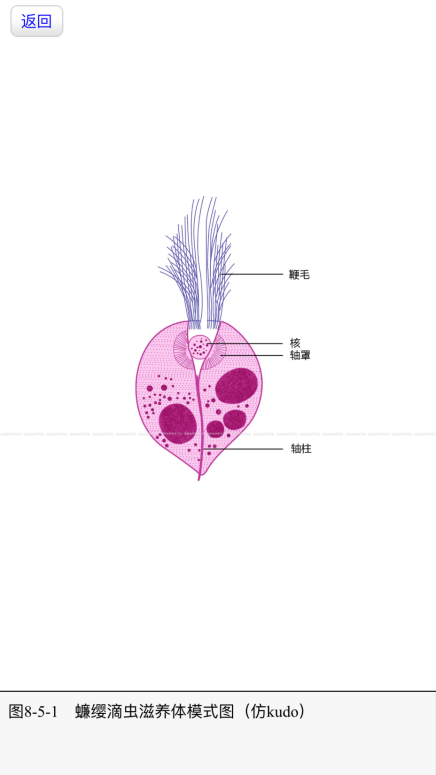
| 滋养体 |
圆形、卵圆形或梨形,一端有成簇的多根鞭毛,泡状细胞核,轴柱前端呈萼状,向后延伸至虫体末端
二分裂繁殖 虫体前端的鞭毛左右不停地摆动,且摆动的方向和幅度都较一致;有的为晃动或泳动;圆形虫体常以自身为中心不停地原地快速打转。 |
 |
||||||||
| 生活史 |
感染方式:滋养体随蜚蠊、白蚁粪便或呕吐物排出,人通过食入或吸入而感染。
原虫主要黏附于支气管黏膜,生长繁殖。主要侵袭支气管、气管、肺等。 |
|||||||||
| 致病与临床 |
临床症状多样,多见于免疫力低下人群(中、老年多见)
寄生于呼吸道:发热、咳嗽、咳痰(量多、色黄、黏液泡沫样) 寄生于支气管肺部:剧烈咳嗽、胸闷、气喘、重症哮喘,无明显胸痛。肺部闻及哮鸣音,X 线肺炎样改变,支气管镜检黏性分泌物。 |
|||||||||
| 诊断与治疗 |
临床上凡见呼吸系统感染而又无明确病因且对抗生素治疗无效者,怀疑本病。
病原学诊断:痰液或肺泡灌洗液,直接涂片查滋养体。 影像学检查:支气管影增粗,肺间质改变,肺泡液渗出,散在大小不等斑片状影支气管镜:受感染的支气管狭窄或闭塞,黏膜粗糙充血肿胀以及支气管管腔内可见“污浊物”、“脓性物”或“痰栓样物”。 原因:蠊缨滴虫不断分裂繁殖、成团生长形成,主要由活虫体、死虫体组成以及支气管黏液、组织细胞。 治疗:甲硝唑或替硝唑 ,静脉注射,复方磺胺甲噁唑,口服 |
|||||||||
寄生虫抗体检查是干扰项:寄生虫感染必须通过形态学方法确诊(镜下找到虫体或虫卵),免疫学方法准确度很差(查抗体可能是现有感染,也可能是既往感染,甚至可能是假阳假阴),部分原因是寄生虫的免疫逃避手段丰富,可能抗体的变化与伪装手段都非常丰富。
幼虫移行途径肺部:粪类圆线虫、钩虫和蛔虫
| 粪类圆线虫 | 概述 | 肠道寄生虫,兼性寄生虫。在寄生世代中,成虫主要在宿主(如人、狗、猫等)小肠内寄生,幼虫可侵入肺、脑、肝、肾等组织器官。 | ||
| 形态 | 在宿主体内的生活阶段包括:成虫,虫卵,杆状蚴,丝状蚴 | |||
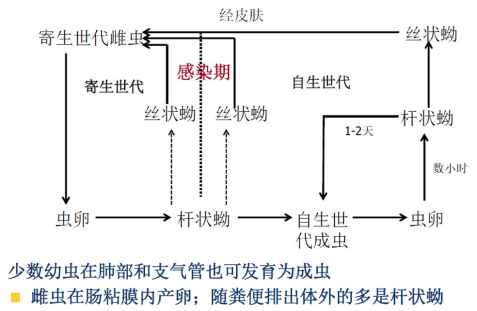
| 生活史 |
人的感染途径:1、外界感染性的丝状蚴经皮肤感染2、体内自身感染3、体外自身感染
当宿主机体免疫力低下或发生便秘时: 体内自身感染 寄生于肠道中的杆状蚴→感染性的丝状蚴 →在小肠下段或结肠经黏膜侵入血循环 体外自身感染 当排出的丝状蚴附着在肛周→钻入皮肤→ 杆状蚴:多随粪便、尿液排出 丝状蚴:多随痰液排出 |
 |
||
| 致病 | 病型:
1、无临床症状 2、间歇出现胃肠症状(慢性自体感染持续存在) 3、播散性重度感染,幼虫进入脑、肝、肺等,导致弥漫性的组织损伤(见于免疫功能低下、免疫抑制剂长期使用者) 皮肤损伤: 引起小出血点、丘疹、并伴有刺痛和痒感,甚至可出现移行性线状荨麻疹。 病变常可反复出现在 肛周、腹股沟、臀部等处皮肤 荨麻疹:蔓延速度快 ,荨麻疹出现的部位及快速蔓延的特点,常是粪类圆线虫幼虫在皮肤移行的重要诊断依据。 肺部症状(丝状蚴移行至肺) 轻感染者:过敏性肺炎或哮喘 重度感染者:咳嗽、多痰、持续性哮喘,呼吸困难,嗜酸性粒细胞增多等 肺部弥漫性感染的病例: 可出现高热、肺功能衰竭。 胸部X线照片: 栗粒状或网状结节样阴影 消化道症状(成虫寄生) 轻者:以小肠黏膜充血为主的卡他性肠炎 重者:水肿性肠炎或溃疡性肠炎,甚至引起肠壁糜 烂,导致肠穿孔。 患者可出现恶心、呕吐、腹痛、腹泻等,并 伴有发热、贫血等症状。 弥漫性粪类圆线虫病 |
|||
| 诊断 |
1.病原学检查:诊断依据为粪便、尿液或痰液任何一类标本找到粪类圆线虫杆状蚴或丝状蚴。间歇排虫:多次检查
注意各类标本的涂片均置于低倍镜下观察,发现可疑虫体再采用碘液染色法转高倍镜辨认。 2.同时出现有消化道和呼吸系统症状的病例,应考虑本病的可能。 3.其他:嗜酸性粒细胞增多;免疫学诊断等 |
|||
| 流行与治疗 |
接触土壤
接触家畜:犬、猫是保虫宿主 激素类、免疫抑制剂使用多 |
治疗药物:阿苯达唑、伊维菌素 | ||
| 蛔虫钩虫幼虫 |
幼虫移行至肺部:支气管肺炎、支气管哮喘
临床表现:咳嗽、胸闷、喉痒、干咳、哮喘、荨麻疹等。 X线:两侧肺门阴影增深,肺纹理增粗,有点状、絮状或片状阴影。 |
|||
总结:(痰液)呼吸系统寄生虫病原检查
1. 直接生理盐水涂片:
适用:卫氏并殖吸虫卵、溶组织内阿米巴滋养体。
要求:受检者晨起后用咳出的气管深处的痰液,勿混入唾液。
2. 消化沉淀法:
收集24小时痰液,加入10% NaOH,痰消化成稀液,离心取沉淀镜检。
适用:卫氏并殖吸虫卵、细粒棘球绦虫原头蚴、蛔蚴、钩蚴、粪类圆线虫幼虫
注意事项:
标本必须是用力咳出的气管深处的痰液,不要混入唾液、鼻咽分泌物、食物、漱口水等;
若主要目的是检查阿米巴滋养体,最好取新鲜痰液快速涂片,并注意玻片保温。
3. 支气管镜检查:支气管肺泡灌洗液。。适用:蠊缨滴虫滋养体
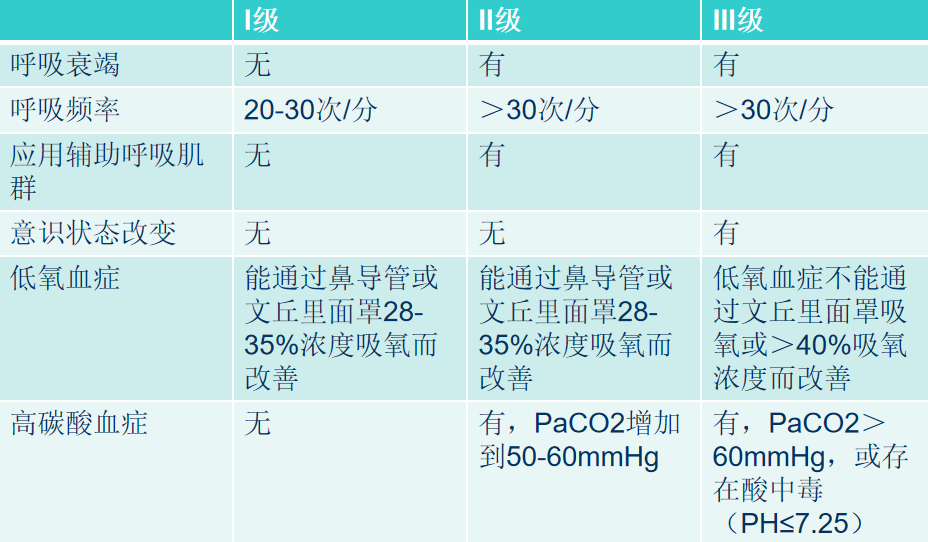
呼吸衰竭
呼吸衰竭:指由各种原因引起肺通气和(或)换气功能严重障碍,以致在静息呼吸状态,吸入空气时,出现低氧血症(PaO₂降低)伴有或不伴有二氧化碳潴留(PaCO₂增高),从而引起机体一系列病理生理改变和临床表现的综合征
发病机制
| 肺泡通气障碍 | 限制性通气不足 | ①呼吸肌活动障碍:呼吸中枢抑制;呼吸肌萎缩,无力等,②胸廓的顺应性降低。③肺的顺应性降低。④胸腔积液和气胸:胸腔大量积液或张力性气胸压迫肺,使肺扩张受限。 | ||
| 阻塞性通气不足 |
①中央性气道阻塞:阻塞若位于胸外,吸气可使气道内压明显低于大气压,导致气道狭窄加重;呼气时减轻,吸气性呼吸困难。如阻塞位于中央气道的胸内部位,患者表现为呼气性呼吸困难。②外周性气道阻塞:慢性阻塞性肺疾患主要侵犯小气道,患者主要表现为呼气性呼吸困难。
肺气肿患者肺泡扩大而数量减少,使细支气管壁上肺泡附着点减少,肺泡壁通过密布的附着点牵拉支气管壁是维持细支气管的形态和口径的重要因素,附着点减少则牵拉力减少,可引起细支气管缩小变形,阻力增加,气道阻塞;呼气性呼吸困难。 |
|||
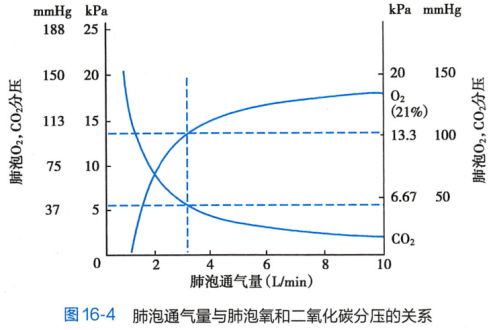
| 血气变化 | PaO₂降低和PaCO₂升高,Ⅱ型呼吸衰竭。 |
 |
||
| 肺换气功能障碍 | 弥散障碍 | ①肺泡膜面积减少:见于肺实变、肺不张、肺叶切除等。②肺泡膜厚度增加:肺水肿、肺泡透明膜形成(主要成分是血浆蛋白和坏死的肺泡上皮碎片)、肺纤维化及肺泡毛细血管扩张等导致血浆层变厚③弥撒时间缩短:体力负荷增加等使心输出量增加和肺血流加快时,血液和肺泡接触时间过于缩短,导致低氧血症。 | ||
| 通气血流比例失调 |
肺的总通气量和总血流量正常,但肺通气或(和)血流不均匀,造成部分肺泡通气与血流比例失调。正常成人在静息状态下,肺泡每分通气量(VA)约为4L,每分钟肺血流量(Q)约为5L,两者的比率(VA/Q)约为0.8。
VA/Q自上而下递减。且随年龄的增长,这种差别更大。 |
|||
| 部分肺泡通气不足 | 支气管哮喘、慢性支气管炎、阻塞性肺气肿等引起的气道阻塞,以及肺纤维化、肺水肿等引起的限制性通气障碍的分布往往是不均匀的,可导致肺泡通气的严重不均。类似动-静脉短路,故称功能性分流,又称静脉血掺杂 | |||
| 血流不足 | 肺动脉栓塞、弥散性血管内凝血、肺动脉炎、肺血管收缩等,VA/Q显著大于正常,称为死腔样通气。正常人肺的生理死腔(VD)约占潮气量(VT)的30%,疾病时,60%~70%,从而导致呼吸衰竭。 | |||
| 解剖分流增加 | 支气管扩张症可伴有支气管血管扩张和肺内动-静脉短路开放,使解剖分流量增加,静脉血掺杂异常增多,而导致呼吸衰竭。解剖分流的血液完全未经气体交换过程,故又称为真性分流。在肺实变和肺不张时,病变肺泡完全失去通气功能,但仍有血流,流经的血液完全未进行气体交换而掺入动脉血,类似解剖分流。吸入纯氧可有效地提高功能性分流的PaO₂,而对真性分流的PaO₂则无明显作用 | |||
1.急性呼吸窘迫综合征(ARDS)与呼吸衰竭:
急性肺损伤(ALI)引起的一种急性呼吸衰竭。如休克、大面积烧伤、败血症等;化学性因素,如吸入毒气、烟雾、胃内容物等;物理性因素,如化学损伤、放射性损伤等;生物因素,如肺部冠状病毒感染引起的严重急性呼吸综合征(SARS)等;或由某些治疗措施,如作体外循环、血液透析等所致。由此可见,ARDS是由不同病因引起的具有明显特征性的急性肺损伤,其损伤特点为弥散性肺泡损伤,特征性病理改变包括肺泡上皮、血管内皮损伤、肺泡膜通透性增加、大量中性粒细胞浸润,肺泡内透明膜形成,以低氧血症和呼吸窘迫为主要临床表现的临床综合征。
发生机制:①致病因子可直接作用②主要通过激活白细胞、巨噬细胞和血小板间接地引起肺损伤;③大量细胞因子[如肿瘤坏死因子α(TNF-α)、白细胞介素(IL-8)、脂多糖(LPS)、补体5a(C5a)、白三烯B4(LTB4)、血栓素A2(TXA2)、血小板活化因子(PAF)、纤维蛋白降解产物(FDPs)]等作用④血管内膜的损伤和中性粒细胞浸润及肺组织释放的促凝物质,导致血管内凝血,形成微血栓,后者通过阻断血流进一步引起肺损伤,通过形成纤维蛋白降解产物及释放TXA2等血管活性物质进一步使肺血管通透性增高。
肺泡-毛细血管膜的损伤及炎症介质的作用使肺泡上皮和毛细血管内皮通透性增高,引起渗透性肺水肿(水肿液富含蛋白)及透明形成,致肺弥散性功能障碍。极端严重病人,由于肺部病变广泛,肺总通气量减少,引起PaCO₂升高,从而导致ARDS患者从I型呼吸衰竭加重为Ⅱ型呼吸衰竭
2.慢性阻塞性肺疾病(COPD)与呼吸衰竭:①阻塞性通气障碍:炎细胞浸润、充血、水肿、黏液腺及杯状细胞增殖、肉芽组织增生引起的支气管壁肿胀;气道高反应性冠、炎症介质作用引起的支气管痉挛;黏液分泌多、纤毛细胞损伤引起的支气管腔堵塞;小气道阻塞、肺泡弹性回缩力降低引起的气道等压点上移。②限制性通气障碍:Ⅱ型上皮细胞受损及表面活性物质消耗过多引起的肺泡表面活性物质减少,营养不良、缺氧、酸中毒、呼吸肌疲劳引起的呼吸肌衰竭。③弥散功能障碍,④肺泡通气与血流比例失调
| 每分通气量(VE) | 指在安静状态下,测定的每分通气量。该指标可以反映肺通气储备功能,VE降低说明肺通气功能损伤严重。 |
| 每分钟肺泡通气量(VA) | 指每分钟肺泡交换气体的体积。VA=(潮气容积-无效腔容积)×呼吸频率,VA可以直接反映有效通气量。 |
| 用力肺活量(FVC) | 和一秒钟用力呼气容积(FEV1)FVC指深吸气后,用力以最快速度所呼出的气体容积,正常在3秒钟内全部呼出。FEV1指深吸气后,用力以最快速度在第一秒呼出的气体容积。FEV1%=FEV1/FVC×100%临床上常用其反映气道阻力。 |
| 最大通气量(MW) | 指每分钟最大和最快深呼吸所测定的通气总量。MVV可以反映气道的动态功能。 |
| 最大呼气中段流量(MMEF) | 指将用力呼出的气体容积分成四等份,其中间呼出气体(即MMEF 25%~75%)的容积除以呼气所需的时间。MMEF可以比较准确地反映气道的阻塞程度,是小气道功能评价的最佳指标。 |
代谢功能变化
一、酸碱平衡及电解质紊乱
(一)代谢性酸中毒
①高血钾;②血清氯浓度增高:代谢性酸中毒时由于HCO;降低,可使肾排Cl-减少
(二)呼吸性酸中毒
呼吸性酸中毒合并代谢性酸中毒时,血Cl-可正常。
(三)呼吸性碱中毒
I型呼吸衰竭时,因缺氧引起肺过度通气,可发生呼吸性碱中毒。此时患者可出现血钾降低,血氯增高。
二、呼吸系统变化
可出现潮式呼吸、间歇呼吸、抽泣样呼吸、叹气样呼吸等呼吸节律紊乱。其中最常见者为潮式呼吸,可能由于呼吸中枢兴奋过低而引起呼吸暂停,从而使血中CO₂逐渐增多,PaCO₂升高到一定程度使呼吸中枢兴奋,恢复呼吸运动,从而排出CO₂,使PaCO₂降低到一定程度又可导致呼吸暂停,如此形成周期性呼吸运动。
在肺顺应性降低所致限制性通气障碍的疾病,因牵张感受器或肺毛细血管旁感受器(J感受器)受刺激而反射性地引起呼吸运动变浅变快。阻塞性通气障碍时,由于气体受阻,呼吸运动加深,由于阻塞的部位不同,表现为吸气性呼吸困难或呼气性呼吸困难。
三、循环系统变化
一定程度的PaO₂降低和PaCO₂升高可兴奋心血管运动中枢,使心率加快、心肌收缩力增强、外周血管收缩,加上呼吸运动增强使静脉回流增加,导致心排血量增加。
呼吸衰竭可累及心脏,主要引起右心肥大与衰竭,即肺源性心脏病。肺源性心脏病的发病机制较复杂:①肺泡缺氧和CO₂潴留所致血液H*浓度过高,可引起肺小动脉收缩(CO₂本身对肺血管起扩张作用),使肺动脉压升高,从而增加右心后负荷;②肺小动脉长期收缩,缺氧均可引起无肌型肺微动脉肌化,肺血管平滑肌细胞和成纤维细胞肥大增生,胶原蛋白与弹性蛋白合成增加,导致肺血管壁增厚和硬化,管腔变窄,由此形成持久而稳定的慢性肺动脉高压;③长期缺氧引起的代偿性红细胞增多症可使血液的黏度增高,也会增加肺血流阻力和加重右心的负荷;④有些肺部病变如肺小动脉炎、肺毛细血管床的大量破坏、肺栓塞等也能成为肺动脉高压的原因;⑤缺氧和酸中毒降低心肌舒、缩功能;⑥呼吸困难时,用力呼气则使胸内压异常增高,心脏受压,影响心脏的舒张功能,用力吸气则胸内压异常降低,即心脏外面的负压增大,可增加右心收缩的负荷,促使右心衰竭。
呼吸衰竭是否可累及左心尚有争论,目前倾向于可累及左心。肺源性心脏病患者心功能失代偿时有半数肺动脉楔压增高,说明有左心功能不全,其中也可能有部分病例合并有冠心病;ARDS的死亡病例中也有半数发生左心衰竭,这些都支持肺部疾病可累及左心的观点。其机制为:①低氧血症和酸中毒同样能使左心室肌收缩性降低;②胸内压的高低同样也影响左心的舒缩功能;③右心扩大和右心室压增高将室间隔向左侧推移,可降低左心室的顺应性,导致左室舒张功能障碍。
四、中枢神经系统变化
PaO₂降至60mmHg时,可出现智力和视力轻度减退。如PaO₂迅速降至40~50mmHg以下,就会引起一系列神经精神症状,如头痛、不安、定向与记忆障碍、精神错乱、嗜睡,以致惊厥和昏迷等。当PaCO₂超过80mmHg时,可引起头痛、头晕、烦躁不安、言语不清、扑翼样震颤、精神错乱、嗜睡、抽搐、呼吸抑制等,即所谓CO₂麻醉。由呼吸衰竭引起的脑功能障碍称为肺性脑病。Ⅱ型呼吸衰竭患者肺性脑病的发病机制与高碳酸血症、酸中毒和缺氧引起的脑水肿和神经元功能障碍有关。
(一)酸中毒和缺氧对脑血管的作用
酸中毒使脑血管扩张,脑充血、水肿,压迫脑血管,更加重脑缺氧,由此形成恶性循环,这也是肺性脑病的发病因素之一。
(二)酸中毒和缺氧对脑细胞的作用
神经细胞内酸中毒一方面可增加脑谷氨酸脱羧酶活性,使γ-氨基丁酸生成增多,导致中枢抑制;另一方面增强磷脂酶活性,使溶酶体水解酶释放,引起神经细胞和组织的损伤
五、肾功能变化
肾受损,轻者尿中出现蛋白、红细胞、白细胞及管型等,严重时可发生急性肾衰竭,出现少尿、氮质血症和代谢性酸中毒。
六、胃肠变化
严重缺氧可使胃壁血管收缩,因而能降低胃黏膜的屏障作用,CO₂潴留可增强胃壁细胞碳酸酐酶活性,使胃酸分泌增多,加之有的患者还可合并弥散性血管内凝血、休克等,故呼吸衰竭时可出现胃肠黏膜糜烂、坏死、出血与溃疡形成等病变。
防治的病理生理基础
一、防止与去除呼吸衰竭的原因
二、提高PaO₂
应尽快将PaO₂提高到50mmHg以上。I型呼衰只有缺氧而无CO₂潴留,可吸入较高浓度的氧。Ⅱ型呼吸衰竭患者的吸氧浓度不宜超过30%,并控制吸氧流速,使PaO₂上升到50~60mmHg
三、降低PaCO₂
①解除呼吸道阻塞②增强呼吸动力③人工辅助通气④补充营养
四、改善内环境及保护重要器官的功能
纠正酸碱平衡及电解质紊乱,保护心、脑、肝和肾等重要器官的功能,预防与治疗严重并发症,如肺源性心脏病与肺性脑病等。
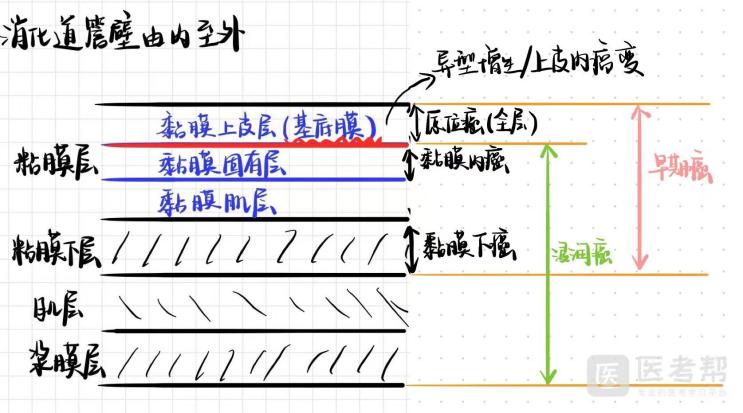
呼吸道病理(肺炎,慢阻塞等)
进行性弥漫性肺泡损伤(DAD)
肺泡-毛细血管屏障急性损伤过度血栓形成和迟发性肺组织和血管重塑组织修复过程受损
肺炎通常指肺的急性渗出性炎症根据病变累及的范围又可称为大叶性肺炎、小叶性肺炎和节段性肺炎。按病变的性质又可分为浆液性、纤维素性、化脓性、出血性、干酪性及肉芽肿性肺炎等。以细菌性肺炎为最常见,大约占肺炎的80%。
| 细菌性肺炎
细菌性肺炎 细菌性肺炎 细菌性肺炎 细菌性肺炎 细菌性肺炎 |
大叶性肺炎
大叶性肺炎 |
概述 |
肺炎球菌引起的以肺泡内弥漫性纤维素渗出为主的炎症,病变通常累及肺大叶的全部或大部。本病多见于青壮年,临床起病急,主要症状为寒战高热、咳嗽、胸痛、呼吸困难和咳铁锈色痰,有肺实变体征及外周血白细胞增多等。淋雨后感染–大叶性肺炎
是纤维素性炎不是纤维素坏死。 |
||
| 发病机制 | 肺炎链球菌引起的,其中1、2、3和7型多见,但以3型毒力最强。进入肺泡内的病原菌迅速生长繁殖并引发肺组织的变态反应,导致肺泡间隔毛细血管扩张、通透性升高,浆液和纤维蛋白原大量渗出 | ||||
| 病理变化及临床病理联系 | 大叶性肺炎的主要病理变化为肺泡腔内的纤维素性炎,常发生于单侧肺,多见于左肺或右肺下叶 | ||||
| 充血水肿期 | 第1~2天:病变肺叶肿胀,暗红色。镜下见肺泡间隔内毛细血管弥漫性扩张充血,肺泡腔内有大量的浆液性渗出液,其内混有少量的红细胞、中性粒细胞和巨噬细胞。渗出液中常可检出肺炎链球菌。此期患者因毒血症而寒战、高热及外周血白细胞计数升高等。胸片X线检查显示片状分布的模糊阴影。 | ||||
| 红色肝样变期 | 第3~4天:肿大的肺叶充血呈暗红色,质地变实,切面灰红,似肝脏外观,故称红色肝样变期。镜下见肺泡间隔内毛细血管仍处于扩张充血状态,而肺泡腔内则充满纤维素及大量红细胞,其间夹杂少量中性粒细胞和巨噬细胞。其中纤维素连接成网并穿过肺泡间孔与相邻肺泡内的纤维素网相连。此期渗出物中仍能检测出较多的肺炎链球菌。X线见大片致密阴影。可出现发绀等缺氧症状。痰液呈铁锈色。病变波及胸膜时,则引起纤维素性胸膜炎,发生胸痛,并可随呼吸和咳嗽而加重。 | ||||
| 灰色肝样变期 |
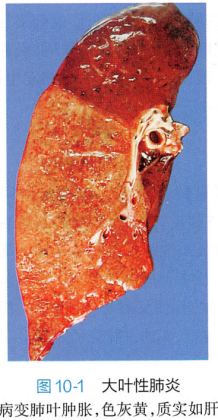
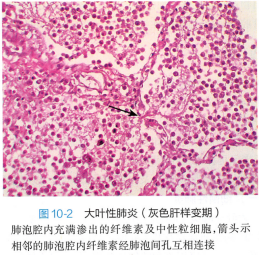
第5~6天:病变肺叶仍肿大,但充血消退,由红色逐渐转变为灰白色,质实如肝,故称灰色肝样变期。镜下见肺泡腔内渗出的纤维素增多,相邻肺泡纤维素丝经肺泡间孔互相连接的现象更为多见。纤维素网中有大量中性粒细胞,因肺泡壁毛细血管受压迫,肺泡腔内几乎很少见到红细胞。
此期肺泡仍不能充气,但病变肺组织内因肺泡间隔毛细血管受压,血流量显著减少,静脉血氧含量不足反而减轻,使缺氧状况得以改善。铁锈色痰逐渐转为黏液脓痰。渗出物中的致病菌除被中性粒细胞吞噬杀灭外,此时机体的特异性抗体已形成,不易检出细菌。 |
  |
|||
| 溶解消散期 | 1周左右:此时机体的防御功能显著增强,病菌消灭殆尽。肺泡腔内中性粒细胞变性坏死,并释放出大量蛋白水解酶将渗出物中的纤维素溶解,由淋巴管吸收或经气道咳出。肺内实变病灶消失,病变肺组织质地较软。肺内炎症病灶完全溶解消散后,肺组织结构和功能恢复正常,胸膜渗出物亦被吸收或机化。患者体温下降,临床症状和体征逐渐减轻、消失,胸部X线检查恢复正常。 | ||||
| 并发症 |
(1)肺肉质变:机化性肺炎。由于肺内炎性病灶中中性粒细胞渗出过少,释放的蛋白酶量不足以溶解渗出物中的纤维素,大量未能被溶解吸收的纤维素即被肉芽组织取代而机化。病变肺组织呈褐色肉样外观,故称肺肉质变。
(2)胸膜肥厚和粘连:纤维素性胸膜炎,若胸膜及胸膜腔内的纤维素不能被完全溶解吸收而发生机化,则致胸膜增厚或粘连。 (3)肺脓肿及脓胸 (4)败血症或脓毒败血症 (5)感染性休克:见于重症病例,是大叶性肺炎的严重并发症。主要表现为严重的全身中毒症状和微循环衰竭,故又称中毒性或休克性肺炎,临床较易见到,死亡率较高。 |
||||
|
小叶性肺炎
小叶性肺炎 |
概述 |
主要由化脓性细菌引起,以肺小叶为病变单位的急性化脓性炎症。病变常以细支气管为中心,故又称支气管肺炎。主要发生于儿童、体弱老人及久病卧床者。
以肺小叶为单位≠一个肺小叶。。下叶和背侧多见,细支气管和肺泡化脓性炎 |
|||
| 病因和发病机制 |
葡萄球菌、肺炎球菌、流感嗜血杆菌、肺炎克雷伯杆菌、链球菌、铜绿假单胞菌及大肠杆菌等。通常是口腔或上呼吸道内的常驻菌。其中致病力较弱的4、6、10型肺炎球菌是最常见的致病菌。当患传染病或营养不良、恶病质、昏迷、麻醉和手术后等情况下,由于机体抵抗力下降,呼吸系统防御功能受损,这些细菌就可能侵入通常无菌的细支气管及末梢肺组织生长繁殖,引起小叶性肺炎。因此,小叶性肺炎常是某些疾病的并发症,如麻疹后肺炎、手术后肺炎、吸入性肺炎、坠积性肺炎等
吸入性、坠积性,手术后肺炎 |
||||
| 病理变化 | 以细支气管为中心的肺组织化脓性炎症。
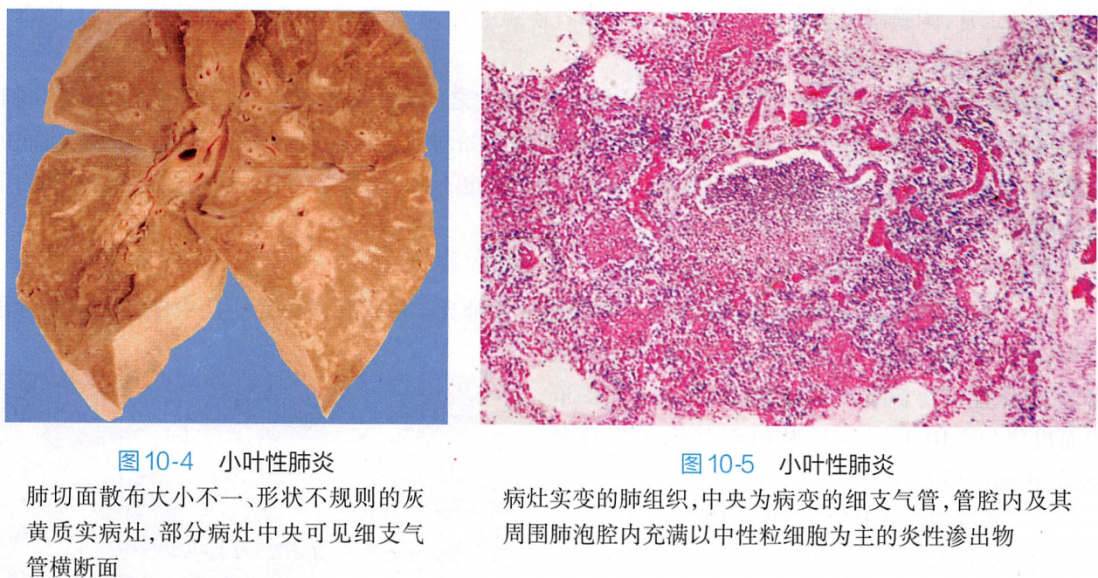
肉眼,双肺表面和切面散在分布灰黄、质实病灶,以下叶和背侧多见。病灶大小不一,直径0.5~1cm(相当于肺小叶范围),形状不规则,病灶中央常可见病变细支气管的横断面。严重病例,病灶可互相融合成片,甚或累及整个大叶,发展为融合性支气管肺炎,一般不累及胸膜。镜下:早期:病变的细支气管黏膜充血、水肿,表面附着黏液性渗出物,周围肺组织无明显改变或肺泡间隔仅有轻度充血。随着病情进展:病灶中支气管、细支气管管腔及其周围的肺泡腔内出现较多中性粒细胞、少量红细胞及脱落的肺泡上皮细胞。充血,可有浆液渗出,部分肺泡过度扩张(代偿性肺气肿)。严重时,病灶中中性粒细胞渗出增多,支气管和肺组织遭破坏,呈完全化脓性炎症改变 |
||||
 |
|||||
| 临床病理联系:为其他疾病的并发症,其临床症状常被原发疾病所掩盖,但发热、咳嗽和咳痰仍是最常见的症状。支气管黏膜受炎症及渗出物的刺激引起咳嗽,痰液往往为黏液脓性或脓性。因病变常呈小灶性分布,故肺实变体征不明显,X线检查则可见肺内散在不规则小片状或斑点状模糊阴影。细支气管和肺泡腔内含有渗出物,听诊可闻及湿啰音。
结局和并发症:经及时有效治疗,本病大多可以痊愈。婴幼儿、年老体弱者,特别是并发其他严重疾病者,预后大多不良。小叶性肺炎的并发症远较大叶性肺炎多,且危险性也大,较常见的有呼吸功能不全、心力衰竭、脓毒血症、肺脓肿和脓胸。并发代偿性肺气肿(支气管扩张) |
|||||
| 病毒性肺炎
病毒性肺炎 |
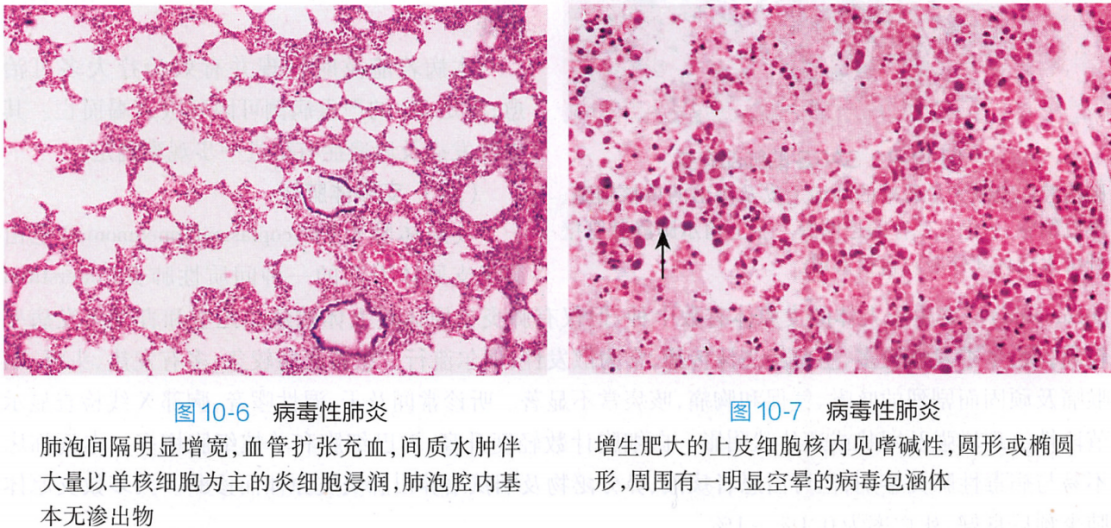
临床症状差别较大,除有发热和全身中毒症状外,还表现为频繁咳嗽、气急和发绀等。
病理变化:主要表现为肺间质的炎症。肺泡间隔明显增宽。由流感病毒、麻疹病毒和腺病毒引起的肺炎,其肺泡腔内渗出的浆液性渗出物常浓缩成薄层红染的膜状物贴附于肺泡内表面,即透明膜形成。细支气管上皮和肺泡上皮也可增生、肥大,并形成多核巨细胞。如麻疹性肺炎时出现的巨细胞较多,又称巨细胞肺炎。在增生的上皮细胞和多核巨细胞内可见病毒包涵体。 病毒包涵体是病毒性肺炎的诊断标准,胞核内:腺病毒、单纯疱疹病毒、巨细胞病毒,胞浆内:呼吸道合胞病毒。。胞核内+胞浆内:麻疹病毒 |
||||
 |
|||||
| 严重急性呼吸综合征(SARS) | 概述 | SARS 起病急,以发热为首发症状,体温一般高于38℃,偶有畏寒,可伴头痛、肌肉和关节酸痛、干咳、少痰,严重者出现呼吸窘迫。外周血白细胞计数一般不升高或降低,常有淋巴细胞计数减少。X 线检查,肺部常有不同程度的块状、斑片状浸润性阴影。 | |||
| 病理变化 | 肺部病变 |
肉眼观双肺呈斑块状实变,严重者双肺完全性实变;表面暗红色,切面可见肺出血
灶及出血性梗死灶。镜下,以弥漫性肺泡损伤为主,肺组织重度充血、出血和肺水肿,肺泡腔内充满大量脱落和增生的肺泡上皮细胞及渗出的单核细胞、淋巴细胞和浆细胞。部分肺泡上皮细胞胞质内可见典型的病毒包涵体,电镜证实为病毒颗粒。肺泡腔内可见广泛透明膜形成,部分病例肺泡腔内渗出物出现机化,呈肾小球样机化性肺炎改变。肺小血管呈血管炎改变,部分管壁可见纤维素样坏死伴血栓形成,微血管内可见纤维素性血栓 |
|||
| 脾和淋巴结 | 体积略缩小,质软。镜下见脾小体高度萎缩,脾动脉周围淋巴鞘内淋巴细胞减少,红髓内淋巴细胞稀疏。白髓和被膜下淋巴组织大片灶状出血坏死。肺门淋巴结及腹腔淋巴结固有结构消失,皮髓质分界不清,皮质区淋巴细胞数量明显减少,常见淋巴组织呈灶状坏死。心、肝、肾、肾上腺等器官除小血管炎症性病变外,均有不同程度变性、坏死和出血等改变。 | ||||
| 支原体肺炎 | 概述 | 肺炎支原体引起的间质性肺炎。秋、冬季,儿童和青少年发病较多,主要经飞沫传播,常为散发性,偶尔流行。起病较急,多有发热、头痛、咽喉痛及顽固而剧烈的咳嗽、气促和胸痛,咳痰常不显著。听诊常闻及干、湿性啰音,胸部X线检查显示节段性纹理增强及网状或斑片状阴影。白细胞计数轻度升高,淋巴细胞和单核细胞增多。本病临床不易与病毒性肺炎鉴别,但可由患者痰液、鼻分泌物及咽拭培养出肺炎支原体而诊断。预后良 | |||
| 病理变化 | 肺部病变常累及一叶肺组织,以下叶多见,偶可波及双肺。病变主要发生于肺间质,故病灶实变不明显,常呈节段性分布。肉眼观呈暗红色,切面可有少量红色泡沫状液体溢出,气管或支气管腔可有黏液性渗出物,胸膜一般不被累及。镜下,病变区内肺泡间隙明显增宽,血管扩张、充血,间质水肿伴大量淋巴细胞、单核细胞和少量浆细胞浸润。肺泡腔内无渗出物或仅有少量混有单核细胞的浆液性渗出液。小支气管、细支气管壁及其周围间质充血水肿及慢性炎细胞浸润,伴细菌感染时可有中性粒细胞浸润。严重病例,支气管上皮和肺组织可明显坏死、出血。 | ||||
铁锈色痰:巨噬细胞吞噬红细胞
心衰细胞:巨噬细胞吞噬含铁血黄素
慢性阻塞性肺疾病
| 慢性支气管炎 | 概述 |
是发生于支气管黏膜及其周围组织的慢性非特异性炎性疾病,要临床特征为反复发作的咳嗽、咳痰或伴有喘息症状,且症状每年至少持续3个月,连续2年以上。病情持续多年者常并发严重影响健康的肺气肿及慢性肺源性心脏病。
道病变引起的主要临床表现是呼气性呼吸困难 |
||
| 发病机制 | ①病毒和细菌感染:多发生于冬春季,鼻病毒、腺病毒和呼吸道合胞病毒,肺炎球菌、肺炎克雷伯杆菌、流感嗜血杆菌等②吸烟:患病率与吸烟量成正比,损伤呼吸道黏膜,降低局部抵抗力,烟雾又可刺激小气道产生痉挛,从而增加气道的阻力。③空气污染与过敏因素④机体内在因素:机体抵抗力降低,呼吸系统防御功能受损及内分泌功能失调等也与本病的发生发展密切相关。 | |||
| 病理变化 | 早期较大的支气管,随病情进展逐渐累及较小的支气管和细支气管。
①呼吸道黏液-纤毛排送系统受损,纤毛柱状上皮变性、坏死脱落,再生的上皮杯状细胞增多,并发生鳞状上皮化生;②黏膜下腺体增生肥大和浆液性上皮发生黏液腺化生,导致分泌黏液增多;③管壁充血水肿,淋巴细胞、浆细胞浸润;④管壁平滑肌断裂、萎缩(喘息型者:平滑肌束增生、肥大),软骨可变性、萎缩或骨化 反复发作必然导致病变程度逐渐加重,累及的细支气管也不断增多,终将引起管壁纤维性增厚,管腔狭窄甚至发生纤维性闭锁;炎症易向管壁周围组织及肺泡扩展,形成细支气管周围炎。 |
|||
| 临床病理联系 | 咳嗽、咳痰。白色黏液泡沫状,在急性发作期,咳嗽加剧,并出现黏液脓性或脓性痰。支气管的痉挛或狭窄及黏液和渗出物阻塞管腔常致喘息。双肺听诊可闻及哮鸣音,干、湿性啰音。某些患者可因支气管黏膜和腺体萎缩(慢性萎缩性气管炎),而痰量减少或无痰。小气道的狭窄和阻塞可致阻塞性通气障碍,此时呼气阻力的增加大于吸气,久之,使肺过度充气,肺残气量明显增多而并发肺气肿。小气道的狭窄和阻塞可致阻塞性通气障碍,此时呼气阻力的增加大于吸气,久之,使肺过度充气,肺残气量明显增多而并发肺气肿。 | |||
|
肺气肿
肺气肿 |
概述 |
是末梢肺组织(呼吸性细支气管、肺泡管、肺泡囊和肺泡)因含气量过多伴肺泡间隔破坏,肺组织弹性减弱,导致肺体积膨大、通气功能降低的一种疾病状态,是支气管和肺部疾病最常见的并发症。
基础病变是细支气管炎和细支气管周围炎,关键性病变是细支气管弹力纤维破坏和官腔不完全阻塞 |
||
| 病因和发病机制 | 阻塞性通气障碍 |
小支气管和细支气管管壁结构遭受破坏及以纤维化为主的增生性改变导致管壁增厚、管腔狭窄;同时黏液性渗出物的增多和黏液栓的形成进一
步加剧小气道的通气障碍,使肺排气不畅,残气量过多。 |
||
| 呼吸性细支气管和肺泡壁弹性降低 | 破坏了大量的弹力纤维,使细支气管和肺泡的回缩力减弱;而阻塞性肺通气障碍使细支气管和肺泡长期处于高张力状态,弹性降低,使残气量进一步增多。 | |||
| α1-抗胰蛋白酶水平降低 |
炎症时,白细胞的氧代谢产物氧自由基等能氧化α1-AT,使之失活,导致中性粒细胞和巨噬细胞分泌的弹性蛋白酶数量增多、活性增强,加剧了细
支气管和肺泡壁弹力蛋白、IV型胶原和糖蛋白的降解,破坏了肺组织的结构,使肺泡回缩力减弱。 |
|||
| 类型 | 肺泡性肺气肿 |
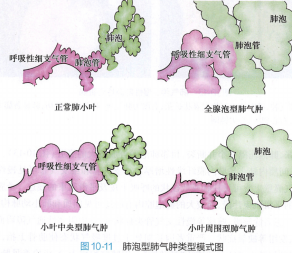
(1)腺泡中央型肺气肿:此型最为常见,多见于中老年吸烟者或有慢性支气管炎病史者。病变特点是位于肺腺泡中央的呼吸性细支气管呈囊状扩张,而肺泡管和肺泡囊扩张不明显。
(2)腺泡周围型肺气肿:也称隔旁肺气肿,此型多 不合并慢性阻塞性肺疾病。腺泡的呼吸性细支气管基本正常,而远侧端位于其周围的肺泡管和肺泡囊扩张。 (3)全腺泡型肺气肿:常见于青壮年、先天性α1-AT缺乏症患者。病变特点是呼吸性细支气管、肺泡管、肺泡囊和肺泡都扩张,含气小囊腔布满肺腺泡内。肺泡间隔破坏严重时,气肿囊腔融合形成直径超过1cm的较大囊泡,则称囊泡性肺气肿 |
 |
|
| 间质性肺气肿 | 肋骨骨折、胸壁穿透伤或剧烈咳嗽引起肺内压急剧增高等均可导致细支气管或肺泡间隔破裂,使空气进入肺间质形成间质性肺气肿。气体出现在肺膜下、肺小叶间隔,也可沿细支气管壁和血管周的组织间隙扩散至肺门、纵隔形成串珠状气泡,甚至可在上胸部和颈部皮下形成皮下气肿。 | |||
| 其他肺气肿 |
①瘢痕旁肺气肿:系指出现在肺组织瘢痕灶周围,由肺泡破裂融合形成的局限性肺气肿,因其出现的具体位置不恒定且大小形态不一,故也称
为不规则型肺气肿,若气肿囊腔直径超过2cm,破坏了肺小叶间隔时,称肺大疱,位于肺膜下的肺大疱破裂可引起气胸。 ②代偿性肺气肿:是指肺萎缩及肺叶切除后残余肺组织或肺炎性实变病灶周围肺组织的肺泡代偿性过度充气,通常不伴气道和肺泡壁的破坏或仅有少量肺泡壁破裂。 ③老年性肺气肿:是因老年人的肺组织弹性回缩力减弱 |
|||
| 病理变化 | 肺的体积显著膨大,色灰白,边缘钝圆,柔软而缺乏弹性,指压后压痕不易消退。切面因肺气肿类型不同,所见囊腔的大小、分布的部位及范围均有所不同,镜下见肺泡扩张,肺泡间隔变窄并断裂,相邻肺泡融合成较大的囊腔。肺泡间隔内毛细血管床数量减少,间质内肺小动脉内膜纤维性增厚。小支气管和细支气管可见慢性炎症改变。肺泡中央型肺气肿的气囊壁上常可见柱状或低柱状的呼吸上皮及平滑肌束的残迹。全腺泡型肺气肿的囊泡壁上偶见残存的平滑肌束片段,而较大的囊泡腔内有时还可见间质和肺小动脉构成的悬梁。 | |||
| 临床病理联系 | 除咳嗽、咳痰等慢性支气管炎症状外,常因阻塞性通气障碍而出现呼气性呼吸困难,气促、胸闷、发绀等缺氧症状。严重者因长期处于过度吸气状态使肋骨上抬,肋间隙增宽,胸廓前后径加大,形成肺气肿患者特有的体征“桶状胸”。因肺容积增大,X线检查见肺野扩大、横膈下降、透明度增加。后期由于肺泡间隔毛细血管床受压迫及数量减少,使肺循环阻力增加,肺动脉压升高,最终导致慢性肺源性心脏病。 | |||
支气管扩张是以肺内小支气管管腔持久性扩张伴管壁纤维性增厚为特征的慢性呼吸道疾病。患者因支气管受慢性炎症及化脓性炎性渗出物的刺激,使患者出现反复咳嗽及咳大量脓痰。临床表现为慢性咳嗽、大量脓痰及反复咯血等症状
(病理)肺尘埃沉着病(不重点)
| 概述 |
长期吸入有害粉尘在肺内沉着,引起以粉尘结节和肺纤维化为主要病变的常见职业病
无机尘肺:硅肺、硅酸盐肺、碳系尘肺、金属尘肺 有机尘肺:农民肺、蘑菇肺、麦芽肺 生产环境中长期吸入大量含游离二氧化硅(SiO2)粉尘微粒引起的以肺纤维化为主要病变的全身性疾病。最严重的一种职业病 |
|
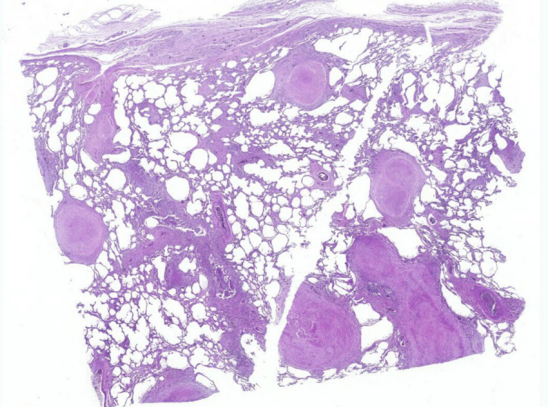
| 核心病变 | 1.硅(矽)结节–基本病变
硅结节(大体) 境界清楚,直径3~5mm,圆形或椭圆形,灰白色,质硬,砂样感,病变发展,结节融合成团块状,团块中央坏死、液化硅肺性空洞。 硅结节(镜下) 细胞性结节(巨噬细胞为主)→纤维性结节(成纤维细胞及胶原纤维为主)→融合性结节及硅肺性空洞 2.肺组织弥漫纤维化 指结节外围的组织发生明显的纤维化,为致密的玻变胶原纤维 |
 |
| 硅肺的分期 |
1.硅结节的数量、大小、分布、
2.肺纤维化的程度 I期硅肺 ·局限在淋巴系统(肺门淋巴结–最早期出现病变的部位–肿大) ·肺组织硅结节量少,直径1~3mm ·肺重量、体积、硬度无明显变化 X线检查肺门阴影增大,密度增强,肺野内可见少量类圆形或不规则形小阴影 II期硅肺 硅结节量增多、体积增大(约1cm)结节散布范围不超过全肺1/3 ·肺重量、体积、硬度均有改变,胸膜增厚 Ⅲ期硅肺 ·硅结节密集融合成块,伴周围肺气肿和肺不张 ·结节散布范围超过全肺1/3 ·肺门淋巴结综合大,呈蛋壳样钙化 ·肺重量、体积、硬度均明显改变(沉水试验阳性),胸膜增厚 |
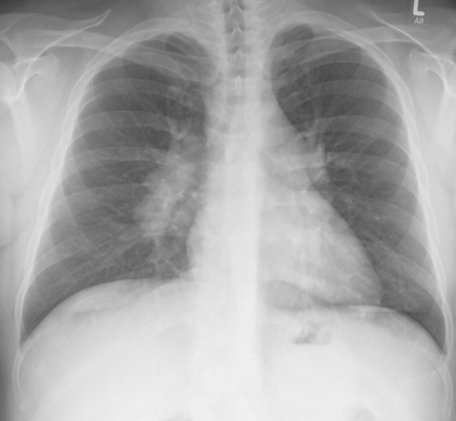 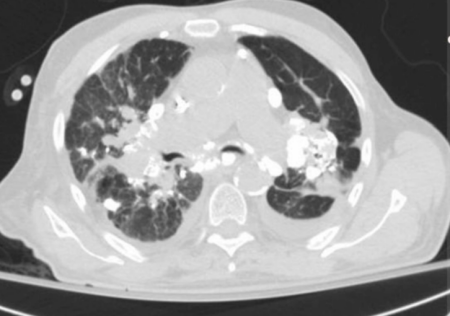 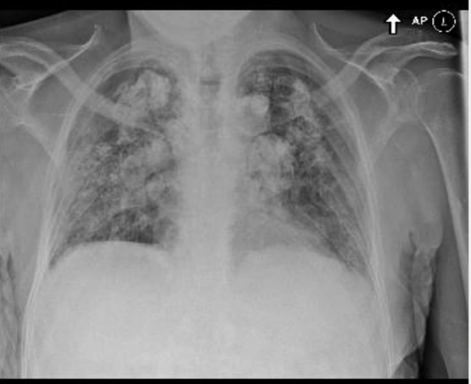 |
| 并发症 |
·肺结核
·慢性肺源性心脏病 ·肺部感染和COPD |
|
即使脱离硅尘环境,已被巨噬细胞吞噬的硅尘可因其破裂而再释放出游离的硅尘,游离的硅尘又可被其他巨噬细胞再吞噬,使其释放多种细胞因子和炎性介质,导致疾病进一步发展,已形成硅结节也可继续诱发机体免疫的发生,因此及时脱离硅尘环境并不能防止病情发展
尘颗粒越小致病力越强,其中以1~2μm者致病性最强
肺动脉高压和肺心病
| 肺动脉高压 | 概述 |
由多种已知或未知原因引起的肺动脉压异常升高的一种病理生理状态,血流动力学诊断标准为:在海平面、静息状态下,右心导管测量平均肺动脉压(mPAP)≥25mmHg(1mmHg=0.133kPa)
肺动脉高压(PAH)是一种以肺血管阻力进行性升高为主的临床综合征 |
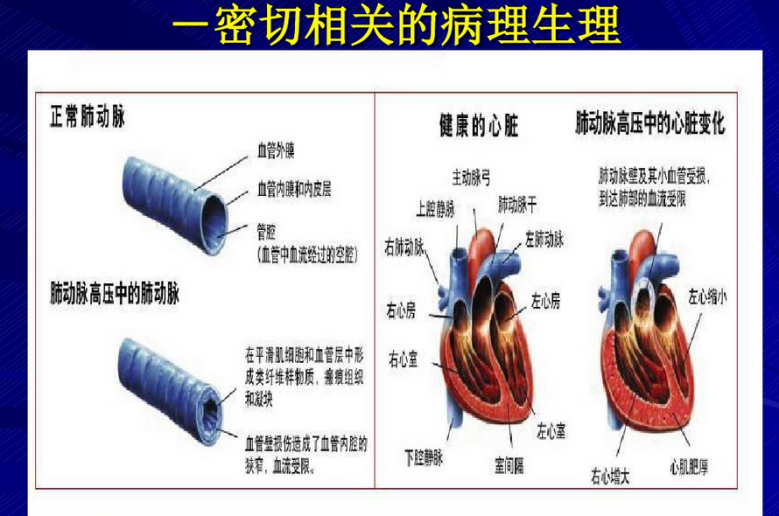 |
|||
| 病因 |
肺动脉血流量增加
& 高动力性肺动脉高压(肺血流量增加) |
(1)左向右分流的先天性心血管异常:房间隔缺损、室间隔缺损、动脉导管未闭。
(2)后天获得性心内分流:主动脉瘤破裂或主动脉瘤破入右心或右心房,心肌梗死后室间隔穿孔。 多见于左向右分流的先天性心脏病或体循环有大的动静脉瘘(Eisenmenger综合征)。 休息时肺循环压大多正常。 在运动时心输出量明显增加,如伴有血管痉挛或血管床减少,则肺动脉压急剧上升。 |
 |
|||
| 肺周围血管阻力增加 | (1)肺血管床缩小:各种原因引起的肺动脉栓塞。a.血管外压迫b.血管本身原因c.血管内栓塞
(2)肺动脉管壁病变: ①肺动脉炎 ③肺动脉先天性狭窄。 ②原发性肺动脉高压:丛性肺血管病、微血栓形成、肺静脉堵塞 ③肺动脉先天性狭窄。 (3)肺纤维化或肺间质肉芽肿: (4)低氧血症致肺血管痉挛: ①慢性阻塞性肺病:慢性支气管炎、 肺气肿、支气管哮喘。 ②呼吸运动障碍:胸膜病、胸廓畸形、多发性脊髓灰质炎、肌萎缩、肥胖症。 ③高原缺氧。 a.自主神经机制b.体液因素(组胺及5-HT,前列腺素F2a和TXA2,ACE,ATII)c.细胞因素(ATP生成减少细胞膜ATP酶活性降低使肺动脉平滑肌丢钾潴钠,致负性膜电位下降,提高了肌肉兴奋性) (5)血黏度改变(原发性红细胞增多症或长期低氧引起继发性红细胞增多症使血液黏度增加) |
|||||
|
肺静脉压增高
& (毛细血管后性肺动脉高压) |
(1)肺静脉堵塞:纵隔肿瘤或肉芽肿病、先天性肺静脉狭窄。
(2)心脏病:左心功能不全、二尖瓣狭窄或闭锁不全、二尖瓣环钙化、左房黏液瘤 二尖瓣病变等,也可发生于长期左室功能不全,左室顺应性低下等。 |
|||||
| 生理 |
血流动力学有以下四个特点:
①压力低:正常静息时肺动脉压力为19/16mmHg,收缩压不超过25mmHg,为主动脉的1/6,肺血管灌注压也低,肺动脉和左心房间压力差仅6mmHg,为正常主动脉压力的l/7~1/10; ②阻力小:因肺血管短、管壁薄、扩张度大,故血流阻力小。正常人肺血管阻力为体循环阻力的1/5~l/10; ③流速快:肺脏接受心脏搏出的全部血液,但其流程远较体循环为短,故流速快; ④容量大:肺血管床面积大,可容纳900mL血液,占全血量的9%。 肺动脉压=肺血管阻力×肺血流量+左心房压力 |
|||||
| 分类 | ||||||
| 机制 | 遗传学机制:骨形成蛋白II型受体(BMPR-II)基因突变
血管活性物质失衡机制:缩血管物质:主要包括TXA2和ET等 舒血管物质:主要包括一氧化氮(NO)和前列环素等 持续的血管收缩和TXA2的比例增加是缺氧诱导的新生儿持续性肺动脉高压的主要特征。 PGI2 缺乏可引起 肺动脉高压。 肺动脉高压时,体内合成NO减少,尤其是肺内组织NO明显减少。 ET与PGI2及NO之间生物学效应存在拮抗作用; ET-1可促进PGI2及NO的合成,而PGI2及NO抑制ET-1的合成。 离子通道机制:特发性肺动脉高压患者与继发性肺动脉高压患者相比,其肺动脉平滑肌细胞Kv明显受到抑制,从而细胞钙离子内流增多,使肺动脉收缩加强,平滑肌细胞增殖 炎症机制:5-HT、白细胞三烯、血小板衍生因子、活性氧代谢产物等,可引起血管收缩。 制最主要的是内皮途径、一氧化氮途径及前列环素途径在内的三大途径 |
|||||
| 对机体的影响 |
(1)劳力性呼吸困难:由于肺血管顺应性下降,心输出量不能随运动而增加,体力活动后呼吸困难往往是肺动脉高压的最早期症状。
(2)乏力:因心输出量下降,组织缺氧的结果。 (3)晕厥:脑组织供血突然减少所致,常见于运动后或突然起立时,也可因大栓子堵塞肺动脉,肺小动脉突然痉挛或心律失常引起。 (4)心绞痛或胸痛:因右心室肥厚冠状动脉灌流减少,心肌相对供血不足。胸痛也可能因肺动脉主干或主分支血管瘤样扩张所致。 (5)咯血:肺动脉高压可引起肺毛细血管起始部微血管瘤破裂而咯血。 (6)声音嘶哑:肺动脉扩张压迫喉返神经所致。 |
|||||
| 防治原则 |
PAH目前仍是一种无法治愈的慢性疾病。
目前PAH的治疗主要分为:1、一般治疗2、 靶向治疗(即针对PAH发病机制本身研发的药物)3、心肺或肺移植4、 姑息治疗 1、一般治疗 1.利尿剂:对存在容量超负荷的肺动脉高压患者给予利尿剂。 2.氧疗:对动脉血氧分压低于60 mm Hg的患者给予吸氧治疗。 3.地高辛:CO低于4 L/min或心搏指数低于2.5L/min/m2是应用地高辛的绝对指征;另外,右心室明显扩张、基础心率大于100次/分、心室率偏快的心房颤动等均是应用地高辛的指征。 4.抗凝治疗:对无抗凝禁忌的特发性肺动脉高压和遗传性肺动脉高压患者 靶向治疗:CCBs、前列环素及其结构类似物、内皮素受体拮抗剂、5型磷酸二酯酶抑制剂和Rho激酶抑制剂等。 |
|||||
| 肺心病 | 病因和发病机制 | 肺疾病 | 慢性阻塞性肺疾病,其中又以慢性支气管炎并发阻塞性肺气肿最常见,其后依次为支气管哮喘、支气管扩张症、肺尘埃沉着病、慢性纤维空洞型肺结核和肺间质纤维化等。肺毛细血管床减少,小血管纤维化、闭塞,使肺循环阻力增加。由于阻塞性通气障碍及肺气血屏障破坏使气体交换面积减少等均可导致肺泡气氧分压降低,二氧化碳分压升高。缺氧引起肺小动脉痉挛,肺血管构型改建,即发生无肌细动脉肌化、肺小动脉中膜增生肥厚等变化。 | |||
| 胸廓运动障碍性疾病 | 重的脊柱弯曲、类风湿关节炎、胸膜广泛粘连及其他严重的胸廓畸形均可使胸廓活动受限而引起限制性通气障碍;也可因肺部受压造成肺血管扭曲、肺萎陷等增加肺循环阻力引起肺动脉压升高及肺心病。 | |||||
| 肺血管疾病 | 原发性肺动脉高压症及广泛或反复发生的肺小动脉栓塞(如虫卵、肿瘤细胞栓子)等可直接引起肺动脉高压,导致肺心病。 | |||||
| 病理变化 | 肺部病变 | 主要病变是肺小动脉的变化,特别是肺腺泡内小血管的构型重建,包括无肌型细动脉肌化及肌型小动脉中膜增生、肥厚,内膜下出现纵行平滑肌束等。肺小动脉炎,肺小动脉弹力纤维及胶原纤维增生,腔内血栓形成和机化以及肺泡间隔毛细血管数量减少等。 | ||||
| 心脏病变 | 心室的病变为主,心室壁肥厚,心室腔扩张,扩大的右心室占据心尖部,外观钝圆。。通常以肺动脉瓣下2cm处右心室前壁肌层厚度超过5mm(正常3~4mm)作为诊断肺心病的病理形态标准。镜下可见右心室壁心肌细胞肥大,核增大、深染;也可见缺氧引起的心肌纤维萎缩、肌浆溶解、横纹消失,间质水肿和胶原纤维增生等。 | |||||
| 临床病理联系 | 呼吸功能不全(呼吸困难、气急、发绀)和右心衰竭(心悸、心率增快、全身淤血、肝脾大、下肢水肿)为其主要临床表现。病情严重者,由于缺氧和二氧化碳潴留,呼吸性酸中毒等可导致脑水肿而并发肺性脑病,出现头痛、烦躁不安、抽搐、嗜睡甚至昏迷等症状。
预防肺心病的发生主要是对引发该病的肺部疾病进行早期治疗并有效控制其发展。右心衰竭多由急性呼吸道感染致使肺动脉压增高所诱发,故积极治疗肺部感染是控制右心衰竭的关键。 |
|||||
| 辅助检查 | ||||||
| 治疗 | ||||||
肺心病的死亡首要原因是肺性脑病,因肺性脑病是最主要的一个并发症,肺性脑病是由于呼吸功能衰竭所致的缺氧,二氧化碳潴留而引起的精神障碍,神经系统症状的综合征,但必须除外脑动脉硬化,严重电解质紊乱,单纯性碱中毒,感染中毒性脑病等。
总结:
慢性肺源性心脏病:(肺小动脉改变)
1⃣️无肌型细动脉肌化
2⃣️肌型小动脉中膜增生、肥厚
3⃣️肺小动脉炎,血栓形成和机化
4⃣️毛细血管数量减少
心脏病变:
1⃣️右心室壁肥厚
2⃣️心腔扩大
3⃣️心肌间质水肿,胶原纤维增生
诊断依据:肺动脉瓣下2cm处右心室壁厚度超过5cm
呼吸窘迫综合征(ARDS)
本病起病急,呼吸窘迫症状不仅重而且难以控制,预后极差
病因和发病机制
本病多继发于严重的全身感染、创伤、休克和肺的直接损伤,如败血症、大面积烧伤、溺水、药物中毒、大量输血或输液、体外循环、透析以及弥漫性肺感染、肺挫伤、吸入性肺炎、吸入有毒气体等,它们均能引起肺毛细血管和肺泡上皮的严重损伤。毛细血管的损伤使管壁通透性升高,导致肺泡内及间质水肿和纤维素大量渗出。肺泡上皮,特别是Ⅱ型上皮损伤后,使肺泡表面活性物质缺失,导致肺泡表面透明膜形成及肺萎陷。上述改变都能造成肺内氧弥漫障碍,气/血比例失调而发生低氧血症,引起呼吸窘迫。
肺毛细血管内皮和肺泡上皮的损伤是由白细胞及某些介质(如白细胞介素、细胞因子、氧自由基、补体及花生四烯酸的代谢产物等)所引起。大量黏附于肺毛细血管内皮细胞上的活化巨噬细胞和中性粒细胞释放氧自由基、蛋白水解酶(如胶原酶、弹力蛋白酶)、血管活性物质(如前列腺素、白细胞三烯、血栓素A2)和血小板激活因子(PAF)等均可导致肺毛细血管广泛而严重的损伤。此外,其中部分介质尚有血管收缩和血小板凝集作用,则进一步减少肺泡血流灌注、加剧气血交换障碍。
病理变化
双肺肿胀,重量增加,暗红色,湿润,可有散在出血点或出血斑。切面膨隆,含血量多,可有实变区或萎陷灶。镜下主要表现为肺间质毛细血管扩张、充血,肺泡腔和肺间质内有大量含蛋白质浆液(肺水肿)。在肺呼吸性细支气管、肺泡管及肺泡的内表面可见薄层红染的膜状物被覆,即透明膜形成。透明膜的成分为血浆蛋白及坏死的肺泡上皮碎屑。间质内可有点状出血和灶状坏死,微血管内常见透明血栓和白细胞栓塞,肺泡上皮弥漫性损伤。电镜下见损伤的Ⅱ型肺泡上皮细胞的线粒体因嵴被破坏而呈空泡变,内质网扩张,板层小体变性、坏死。发病数日后即可见肺间质内成纤维细胞及Ⅱ型肺泡上皮大量增生,透明膜机化和胶原沉着,导致肺泡和肺间质弥漫性纤维化。
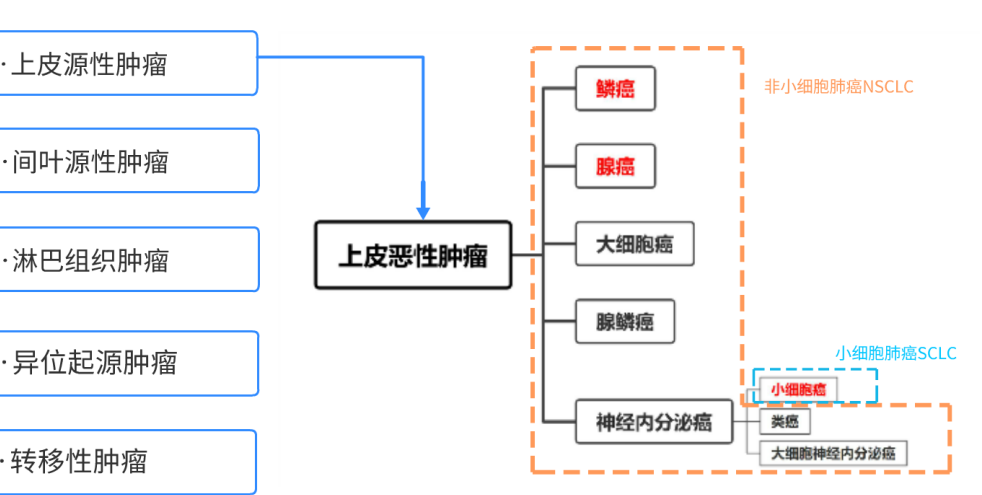
(病理)肺癌
大叶性肺炎——铁锈色痰
小叶性肺炎——黏液脓性或脓性痰
慢性支气管炎——白色黏液泡沫痰
支气管扩张症——大量脓痰 咯血
粉红色泡沫痰——肺水肿
肺癌——早期 咳嗽、痰中带血,胸痛
病因
| 吸烟 | 与吸烟的量和吸烟时间的长短正相关。 |
| 空气污染 | 与交通工具或工业排放的废气或粉尘污染空气密切相关,污染的空气中3,4-苯并芘、二乙基亚硝酸胺及砷等致癌物的含量均较高。 |
| 职业因素 | 事某些职业的人群,如长期接触放射性物质(铀)或吸入含石棉、镍、砷等化学致癌粉尘的工人,肺癌发生率明显增高。 |
| 分子遗传学改变 |
如KRAS基因突变:该突变与腺癌的预后不良有关。
c-MYC基因的活化(过度表达):小细胞癌 p53和Rb |
| 概述 |
·起源:大多为支气管粘膜上皮。发病率和死亡率有增加趋势。
·好发年龄:40-70岁,男多于女。 |
| 中央型肺癌 |
·发生于主支气管或叶支气管
·常形成围绕支气管的在肺门附近形成巨大肿块,病变气管壁可弥漫增厚或形成息肉状或乳头状肿物突向管腔,使气管腔狭窄或闭塞。随病情进展,肿瘤破坏气管壁向周围肺组织浸润,扩展,在肺门部形成包绕支气管的巨大肿块 |
| 周围型肺癌 | ·发生于段以下支气管,位于肺周边部。单发或多发结节,与周围组织分界较清。易侵及胸膜,与支气管关系不明显。占30-40%。起源于肺段或其远端支气管,在靠近肺膜的肺周边部形成孤立的结节状或球形癌结节 |
| 弥漫型肺癌 | 肿瘤体积小,弥漫浸润,可累及全肺。外观似大叶性肺炎或融合性小叶性肺炎。起病隐匿,病程长。占2-5%。源于末梢的肺组织,沿肺泡管及肺泡弥漫性浸润生长,形成多数粟粒大小结节布满大叶的一部分或全肺叶;也可形成大小不等的多发性结节散布于多个肺叶内,易与肺转移癌混淆。 |
| 隐匿型肺癌 | 早期肺癌:中央型~:腔内生长或管壁浸润,未突破外膜侵及肺实质,无局部淋巴结转移。周围型~:结节状,直径<2cm,无局部淋巴结转移。–早期症状无意义
隐性肺癌:临床及X线检查(-),痰细胞学检查癌细胞(+)。手术切除标本病理证实为原位癌或早期浸润癌而无淋巴结转移。 |
组织学特性
恶性程度:从小到大显(腺)得另(鳞)类(类癌)
金标准:纤维支气管镜活检
|
腺癌
腺癌 |
女性肺癌最常见的类型,多为非吸烟者。较小支气管上皮,故大多数为周围型肺癌。肿块通常位于胸膜下,境界不甚清晰,常累及胸膜,腺癌伴纤维化和瘢痕形成较多见,有人称此为瘢痕癌(特殊)
·多发生于段以下支气管 ·肿块位于肺外周 |
原位腺癌(AIS)、微浸润性腺癌(MIA)和浸润性腺癌。AIS被定义为局限性,肿瘤细胞沿肺泡壁呈鳞屑样生长,无间质、血管或胸膜浸润的小腺癌(≤3cm)。
MIA则被定义为孤立性、以鳞屑样生长方式为主且浸润灶≤0.5cm的小腺癌(≤3cm)。浸润性腺癌其浸润灶>0.5cm。浸润性腺癌按分化程度,可分为高、中、低分化三类。高分化腺癌主要表现为癌细胞沿肺泡壁、肺泡管壁,有时也沿细支气管壁呈鳞屑样生长;肺泡间隔大多未被破坏,故肺泡轮廓依然保留。中分化肺腺癌根据腺管、乳头或黏液分泌等形态特征在癌组织中所占比例又可分为腺泡型、乳头状和实体黏液细胞型等亚型。低分化肺腺癌常无腺样结构,呈实心条索状,分泌现象少见,细胞异型性明显。 |
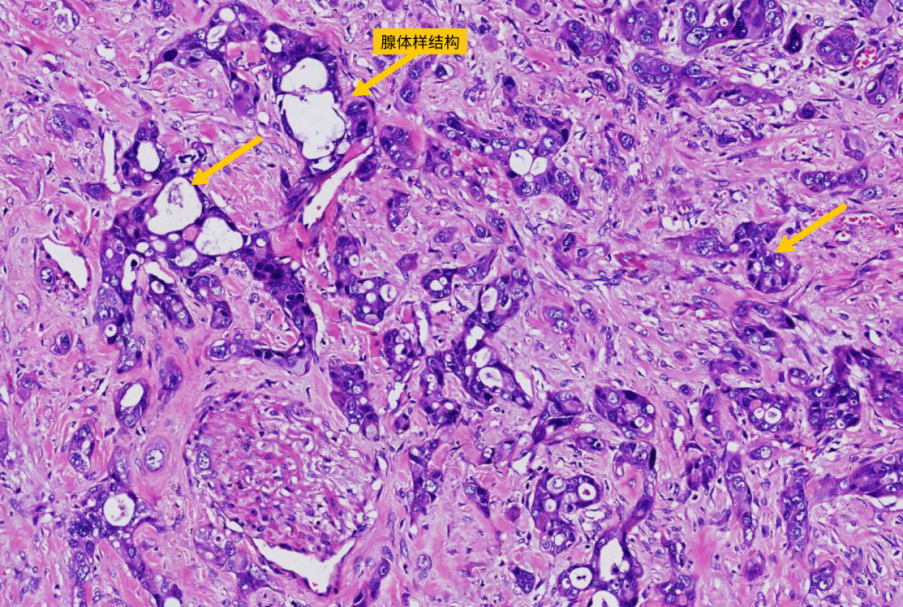 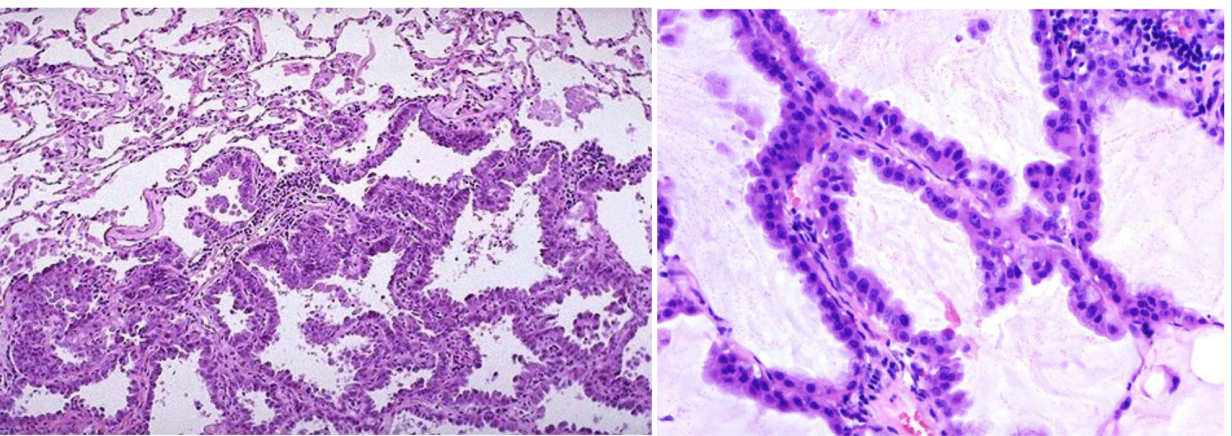 5-30mm的纯磨玻璃结节(pGGN),密度均匀,CT值在-600以下,极少有空泡、毛刺、胸膜牵拉和分叶,可以有血管穿过,但无血管弯曲。 如何鉴别肺部的原发性腺癌与转移性腺癌? TTF-1(甲状膜录因子-1)+ TG(甲状腺球蛋白)- NapsinA(新天冬氨酸蛋白酶A)+ CK7(角蛋白7) |
||
| 鳞状细胞癌 | 最常见,与吸烟关系明显,起源于段以上支气管,80-85%为中央型。分为高、中、低分化鳞癌,中分化者最多。
可分为角化型、非角化型和基底细胞样型。角化型癌巢中有角化珠形成,常可见细胞间桥;非角化型无角化珠形成,细胞间桥也很难见到;基底细胞样型是癌细胞较小,质少,似基底细胞样的形态,且癌巢周边的癌细胞呈栅栏状排列. |
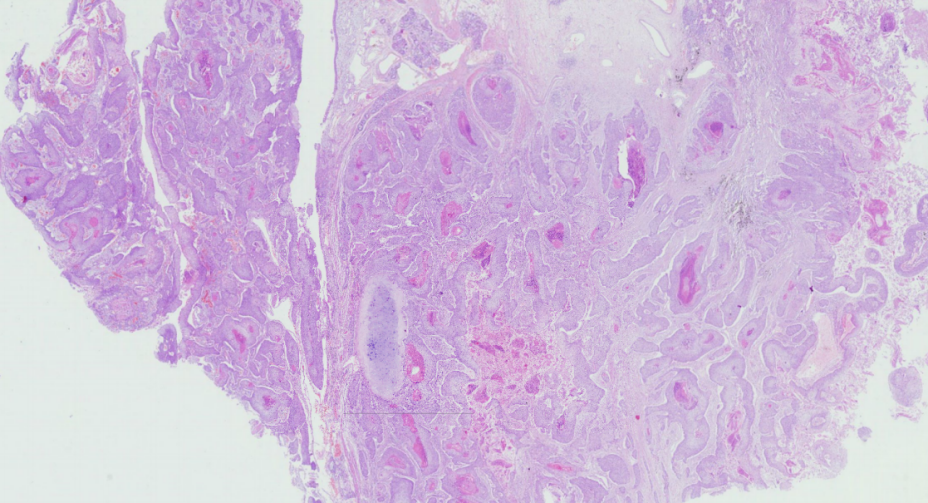 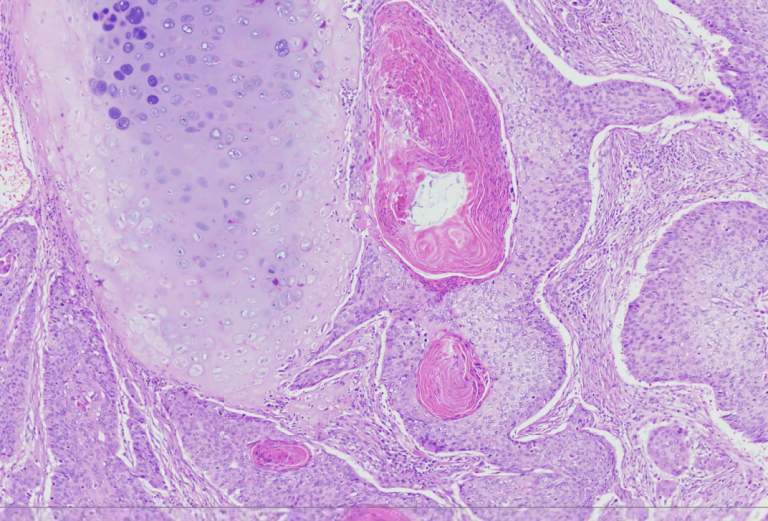 |
| 神经内分泌癌 | (小细胞癌)–大部分中央型(和吸烟的相关性更大)·占10-20%,中老年男性多,多位于肺门部
,生长迅速,转移早,恶性度最高,放化疗敏感,起源于支气管粘膜上皮的神经内分泌细胞(PNEC)【肺神经内分泌细胞(PNEC):位于大气道分支点的气道上皮内,仅占总数1%,受传入和传出神经支配,感受化学和机械刺激,并调节局部免疫反应】 |
常发生于大支气管,向肺实质浸润生长,形成巨块。镜下,癌细胞小,常呈圆形或卵圆形,似淋巴细胞,但体积较大;也可呈梭形或燕麦形,胞质少,似裸核,癌细胞呈弥漫分布或呈片状、条索状排列,称燕麦细胞癌;有时也可围绕小血管形成假菊形团结构。电镜下胞质内可见神经分泌颗粒(可分泌激素–副肿瘤综合征)
免疫组化:神经元特异性烯醇化酶(NSE)、嗜铬蛋白 A(CgA)、突触素(Syn)及人自然杀伤细胞相关抗原(Leu7)等呈阳性反应,角蛋白亦可显示阳性。CD56(神经细胞黏附分子)+  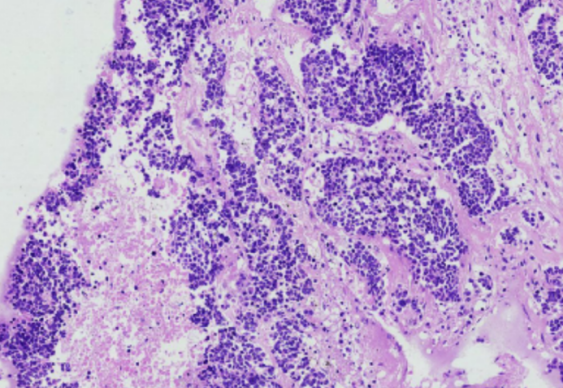 |
| 大细胞癌 | 大细胞未分化癌。半数大细胞癌发生于大支气管,肿块常较大。镜下,癌 细胞常呈实性团块或片状,或弥漫分布。癌细胞体积大,胞质丰富,通常均质淡染,也可呈颗粒状或胞质透明。核圆形、卵圆形或不规则形,染色深,异型性明显,核分裂象多见。癌组织无任何腺癌、鳞癌或神经内分泌癌分化的组织学形态特点及免疫表型。大细胞肺癌恶性程度高,生长迅速,转移早而广泛,生存期大多在1年之内。 | |

扩散途径
1.直接蔓延:侵及纵隔或对侧肺。侵犯胸膜和胸壁。
2.转移
淋巴道:肺门淋巴结→纵隔淋巴结、锁骨上淋巴结和颈部淋巴结。
血道:肝、脑、肾上腺、骨及肾
种植:胸腔内种植转移
临床病理联系:咳嗽、咯血、胸痛,压迫症状,副肿瘤综合征(如类癌综合征)
预后:与组织学类型、癌细胞分化和分期有关。
肺→骨,脑
胃→肝,肺,骨
肝→肝内血行,肺(肝外血行) ,肝门(淋巴)
肠→肝,肺,骨
分子病理
·针对所有II期以后,所有含腺癌成分的NSCLC
·常规筛查表皮生长因子受体EGFR,间变性淋巴瘤激酶ALK,肉瘤致癌因子-受体酪氨酸激ROS1三个基因的突变情况
·若以上三个基因无突变,则检查扩展基因突变情况BRAF、
MET、HER2、KRAS、RET等
·免疫组织化学检测PD-L1表达情况、
EGFR基因突变的影响(以19号外显子缺失突变为例)
突变产生的蛋白会激活酪氨酸激酶受体相关通路,引发肿瘤细胞增殖和迁移酪氨酸激酶抑制剂(TKI,xx替尼)是截断上述过程的靶向药物
该突变在亚洲人群中占30%-50%,也是女性非吸烟肺癌患者的常见突变类型突变患者虽对靶向药物敏感,但对常规化疗药物不敏感
一段时间后,多数患者会出现对靶向药的耐药
总体而言,EGFR突变患者应用靶向药物后,总体生存率依然比接受常规化疗的非突变患者要高

1.周围型:腺癌
2.中央型:鳞癌,小细胞癌,大细胞癌
3.弥漫型:细支气管-肺泡细胞癌(高分化腺癌),鳞、小、大 中央型
高分化腺癌—即—细支气管肺泡癌
弥漫鳞癌小细胞癌多中央型,高分化腺癌细支气管肺泡癌肺泡细胞癌多弥漫
小细胞癌常位于肺中心部,早期多已转移到肺门和纵膈淋巴结,,,对放化疗敏感,预后最差!!!
胸部体格检查
四角,四窝,
胸骨角:胸骨柄和体的连接处–第二肋(计数)——标志:支气管分叉,心房上缘,上下纵隔交接,相当于第五胸椎水平
腹上角:胸骨下和肋弓的角70-100°:对应肝左叶,胃,胰,剑突
肩胛下角:对应第七第八肋间水平,(作胸穿) 脊突-7颈椎,
肋脊角:脊柱和第十二肋夹角
四窝(自然)
胸骨上窝:检查气管是否居中
锁骨上窝:第二肺尖上部
肋间隙
腋窝
八线:
锁骨中线,前正中线,胸骨线,腋前线,腋中线,腋后线,后正中线,肩胛线(双臂下垂)
肺和胸膜分界:肺尖:距锁骨上缘3cm.第一胸椎,肺上界,肺外侧界,肺下界(始于第六肋,锁骨中线-6,腋中线-8,肩胛线-10)
视诊:胸壁静脉(怒张),皮下气肿(气胸等),肋间隙(回缩,三凹征,膨隆-胸腔积液),
异常呼吸:胸式和腹式呼吸,吸气性(大气道),呼气性(COPD等小气道)
呼吸浅快(呼吸机麻痹,腹水,肥胖,严重鼓肠)//深快(剧烈运动,紧张,代酸)
呼吸节律:正常呼>吸=2:1
异常:
潮式呼吸(中枢疾病–间歇呼吸暂停),
危重
间停呼吸(Biots呼吸,中枢兴奋降低-潮式呼吸恶化)
抑制性呼吸–因疼痛
叹气样呼吸-精神紧张
触诊
前/后胸廓扩张度:双手,放于肋弓,拇指向剑突,嘱患者深吸气,观察拇指扩张度(对称)
后:第十肋水平
临床意义:一侧减弱:胸腔积液,气胸,肺炎,肺不张等,双侧-肺气肿
语颤:交叉检查,嘱患者发出“一”声,上到下,内到外。双侧对比
增强–肺实变(大叶性肺炎,浅在大空洞),减弱-气量增多(肺气肿,气管阻塞,积液)
胸膜摩擦感-胸膜炎,吸气摩擦,胸部前下明显
叩诊:清音(正常),浊音(充水,肺炎,肿瘤),实音,鼓音(正常胃泡鼓音区,病理空腔:脓肿,结核,气胸)
肺上界-肺尖宽度:增宽见于结核
肺下界:平静呼吸:锁骨中线-6,腋中线-8,肩胛线-10
降低见于COPD
肺下界移动度叩诊:深吸气和深呼气后屏气,后叩诊,正常间距为6-8cm
异常:胸膜粘连,纤维化
支气管呼吸音
支气管肺泡呼吸音
啰音:干啰音(气道受阻,双侧性-支气管炎,哮喘;单侧-结核,肿瘤=】
),湿罗音(液体)
哨笛音(音调高,乐音性,小支气管),鼾音


2025-05-12-1024x1024.png)